摘要:已知反应前后混合气体的体积.求混合物所含成分体积分数时,
网址:http://m.1010jiajiao.com/timu3_id_337420[举报]
已知烯烃X和炔烃Y常温下为气体,烯烃X和足量的O2的混合气体充分燃烧前后体积不变(100 ℃以上,同温同压下)。现取烯烃X和炔烃Y与足量O2共1.12 L,充分燃烧后,气体总体积为1.17 L(100 ℃以上,同温同压下测定,除去未反应的氧气)。求:
(1)烯烃X的分子式;
(2)炔烃Y的分子式;
(3)1.12 L混合气体中,所允许烯烃X的最大体积(保留4位小数)。
查看习题详情和答案>>(1)已知H2O(l)=H2O(g);△H=+44KJ/mol.在25℃、101kPa下,1g甲醇燃烧生成CO2和气态水时放热19.93kJ,则该反应的热化学方程式应为______.
(2)已知H2的燃烧热△H=-285.8kJ?mol-1,CO的燃烧热△H=-282.8kJ?mol-1.现有CO、H2、CO2组成的混合气体67.2L(标准状况),经充分燃烧后放出的总热量为710.0kJ,并生成18g液态水,求燃烧前混合气体中CO的体积分数.______.
查看习题详情和答案>>
(2)已知H2的燃烧热△H=-285.8kJ?mol-1,CO的燃烧热△H=-282.8kJ?mol-1.现有CO、H2、CO2组成的混合气体67.2L(标准状况),经充分燃烧后放出的总热量为710.0kJ,并生成18g液态水,求燃烧前混合气体中CO的体积分数.______.
 运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.
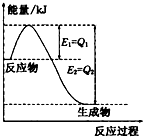
运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.(1)如图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式(△H的数值用含字母Q1、Q2的代数式表示):
N2(g)+3H2(g)═2NH3(g)△H=2(Q1-Q2)kJ?mol-1
N2(g)+3H2(g)═2NH3(g)△H=2(Q1-Q2)kJ?mol-1
(2)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定--氨的电解法合成,大大提高了氮气和氢气的转化率.总反应式为:N2+3H2
| ||
| (一定条件) |
阳
阳
极(填“正”、“负”、“阴”或“阳”);在另一电极通入N2,该电极反应式为N2+6H++6e-=2NH3
N2+6H++6e-=2NH3
.(3)氨气溶于水得到氨水.在25℃下,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合(混合后体积为混合前体积之和),反应后溶液显中性.求25℃下该混合溶液中氨水的电离平衡常数
| b×10-7 |
| a-b |
| b×10-7 |
| a-b |
(4)已知:25℃时KSP(AgCl)=1.6×l0-10 KSP(AgI)=1.5×l0-16
海水中含有大量的元素,常量元素如氯,微量元素如碘,其在海水中均以化合态存在.在25℃下,向0.1L0.002mol?L-l的NaCl溶液中逐滴加入适量的0.1L0.002mol?L-l硝酸银溶液,有白色沉淀生成,从难溶电解质的溶解平衡角度解释产生沉淀的原因是
c(Ag+)?c(Cl-)>Ksp(AgCl)
c(Ag+)?c(Cl-)>Ksp(AgCl)
,向反应后的浑浊液中继续加入0.1L0.002mol?L-1的NaI溶液,看到的现象是白色沉淀转化为黄色沉淀
白色沉淀转化为黄色沉淀
,产生该现象的原因是(用离子方程式表示)AgCl(s)+I-(aq)═AgI(s)+Cl-(aq)
AgCl(s)+I-(aq)═AgI(s)+Cl-(aq)
.