摘要:25.通过案例分析.归纳检查装置气密性的一般方法?
网址:http://m.1010jiajiao.com/timu3_id_337292[举报]
比较、分析、归纳是学习化学的有效方法。现有反应:
①Zn+CuCl2====ZnCl2+Cu;②Cu+2AgNO3====Cu(NO3)2+2Ag; ③Cl2+2NaBr====2NaCl+Br2;
④Br2+2NaI====2NaBr+I2。
(1)通过比较、分析,可以发现上述四个反应有相似之处:均属于四种基本反应类型中的______反应。再分析这四个反应前后各元素的化合价,我们还会发现一个相似之处:________________。
(2)分析反应①和②,可以得到:Zn、Cu、Ag三种金属的活动性由强到弱的顺序是_____________。根据反应③和④,用相似的思维方法,试判断将Cl2通入KI溶液中能否发生反应?若能发生反应请写出化学方程式,若不能发生反应请简述理由__________________________。
查看习题详情和答案>>
①Zn+CuCl2====ZnCl2+Cu;②Cu+2AgNO3====Cu(NO3)2+2Ag; ③Cl2+2NaBr====2NaCl+Br2;
④Br2+2NaI====2NaBr+I2。
(1)通过比较、分析,可以发现上述四个反应有相似之处:均属于四种基本反应类型中的______反应。再分析这四个反应前后各元素的化合价,我们还会发现一个相似之处:________________。
(2)分析反应①和②,可以得到:Zn、Cu、Ag三种金属的活动性由强到弱的顺序是_____________。根据反应③和④,用相似的思维方法,试判断将Cl2通入KI溶液中能否发生反应?若能发生反应请写出化学方程式,若不能发生反应请简述理由__________________________。
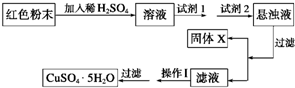 某校一化学实验小组通过实验分析,确定一红色粉末为Fe2O3和Cu2O的混合物.
某校一化学实验小组通过实验分析,确定一红色粉末为Fe2O3和Cu2O的混合物.己知:①Cu2O溶于稀硫酸生成Cu和CuSO4,②Cu2O在空气中加热生成CuO.
(1)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为
| 100(b-a) |
| a |
| 100(b-a) |
| a |
(2)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4?5H2O).经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | 供选择试剂 | |
| Fe3+ | 1.9 | 3.7 | A.氯水,B.H2O2, C.NaOH,D.氨水, E.CuO,F.Cu2(OH)2CO3 |
| Fe2+ | 7.5 | 11 | |
| Cu2+ | 6.0 | 10 |
试回答:
①试剂1可以为
B
B
,试剂2可以为EF
EF
.②固体X的化学式为
Fe(OH)3
Fe(OH)3
.③操作Ⅰ为
蒸发浓缩、冷却结晶
蒸发浓缩、冷却结晶
.(2013?浙江模拟)K3[Fe(C2O4)3]?3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂.实验室可用铁屑为原料制备,相关反应的化学方程式如下,请回答下列问题:
Fe(s)+H2SO4═FeSO4+H2↑
FeSO4+H2C2O4+2H2O═FeC2O4?2H2O↓+H2SO4
2FeC2O4?2H2O+H2O2+H2C2O4+3K2C2O4═2K3[Fe(C2O4)3]+6H2O
2Mn
+5C2
+16H+═2Mn2++10CO2↑+8H2O
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收.下列吸收装置正确的是

(2)在得到的FeSO4溶液中需加入少量的H2SO4酸化,目的是
在将Fe2+氧化的过程中,需控制溶液温度不高于40℃,理由是
得到K3[Fe(C2O4)3]溶液后,加入乙醇的理由是
(3)析出的K3[Fe(C2O4)3]晶体通过如 图所示装置的减压过滤与母液分离.
图所示装置的减压过滤与母液分离.
下列操作不正确的是
A.选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸
B.放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤
C.洗涤晶体时,先关闭水龙头,用蒸馏水缓慢淋洗,再打开水龙头抽滤
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,以防倒吸
(4)晶体中所含结晶水可通过重量分析法测定,主要步骤有:
①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复②~④至恒重,⑥计算.
步骤③需要在干燥器中进行,理由是
(5)晶体中C2
含量的测定可用酸性KMnO4标准溶液滴定.滴定过程中发现,开始时滴入1滴KMnO4标准溶液,紫红色褪去很慢,滴入一定量后,紫红色很快褪去,理由是
(6)下列关于酸式滴定管的使用,正确的是
A.滴定管用蒸馏水洗涤后,即可装入标准溶液
B.装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量酸液,使尖嘴充满酸液
C.滴定管中溶液体积应读数至小数点后第二位
D.接近终点时,需用蒸馏水冲洗瓶壁和滴定管尖端悬挂的液滴.
查看习题详情和答案>>
Fe(s)+H2SO4═FeSO4+H2↑
FeSO4+H2C2O4+2H2O═FeC2O4?2H2O↓+H2SO4
2FeC2O4?2H2O+H2O2+H2C2O4+3K2C2O4═2K3[Fe(C2O4)3]+6H2O
2Mn
| O | - 4 |
| O | 2- 4 |
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收.下列吸收装置正确的是
A
A
.
(2)在得到的FeSO4溶液中需加入少量的H2SO4酸化,目的是
防止Fe2+的水解
防止Fe2+的水解
;在将Fe2+氧化的过程中,需控制溶液温度不高于40℃,理由是
防止H2O2分解
防止H2O2分解
;得到K3[Fe(C2O4)3]溶液后,加入乙醇的理由是
三草酸合铁酸钾在乙醇中溶解度小
三草酸合铁酸钾在乙醇中溶解度小
.(3)析出的K3[Fe(C2O4)3]晶体通过如
 图所示装置的减压过滤与母液分离.
图所示装置的减压过滤与母液分离.下列操作不正确的是
BC
BC
.A.选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸
B.放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤
C.洗涤晶体时,先关闭水龙头,用蒸馏水缓慢淋洗,再打开水龙头抽滤
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,以防倒吸
(4)晶体中所含结晶水可通过重量分析法测定,主要步骤有:
①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复②~④至恒重,⑥计算.
步骤③需要在干燥器中进行,理由是
防止吸水
防止吸水
;步骤⑤的目的是检验晶体中的结晶水是否已全部失去
检验晶体中的结晶水是否已全部失去
.(5)晶体中C2
| O | 2- 4 |
生成的Mn2+起催化作用
生成的Mn2+起催化作用
.(6)下列关于酸式滴定管的使用,正确的是
BC
BC
.A.滴定管用蒸馏水洗涤后,即可装入标准溶液
B.装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量酸液,使尖嘴充满酸液
C.滴定管中溶液体积应读数至小数点后第二位
D.接近终点时,需用蒸馏水冲洗瓶壁和滴定管尖端悬挂的液滴.
Ⅰ、有以下数据,请你通过观察分析,得出相应的结论填在空白处.
结论:
Ⅱ、
(1)0.5mol H2SO4中含
(2)9.03×1023个CO2的物质的量是
(3)3.01×1023个OH-的质量为
查看习题详情和答案>>
| 化学式 | Fe | NaCl | H2O | H2 |
| 相对原子质量或相对分子质量 | 56 | 58.5 | 18 | 2 |
| 1mol物质的质量 | 56g | 58.5g | 18g | 2g |
1mol物质的质量,以克为单位时,数值上等于该物质的相对原子质量或相对分子质量
1mol物质的质量,以克为单位时,数值上等于该物质的相对原子质量或相对分子质量
Ⅱ、
(1)0.5mol H2SO4中含
2
2
mol O.(2)9.03×1023个CO2的物质的量是
1.5mol
1.5mol
,标准状况下的体积为33.6
33.6
L,质量是66
66
克.(3)3.01×1023个OH-的质量为
8.5克
8.5克
,含有电子的物质的量为5mol
5mol
.现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、A
、M
、B
、F
和五种阴离子Cl-、OH-、N
、C
、X中的一种.
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是 和 (填化学式).
(2)为了确定X,观将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕灰色沉淀,向该沉淀中滴入稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解.则:
①X为 .
A.S
B.S
C.CH3COO- D.Si
②A中的化学键类型为 .
③B的水溶液中所有离子的浓度由大到小的顺序为 (用离子符号表示).
④将0.02mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为 (精确到0.1g).
⑤利用上述已经确定的物质,可以检验出D、E中的阳离子.请简述实验操作步骤、现象及结论: .
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.则物质D一定含有上述离子中的 (填相应的离子符号).有关反应的离子方程式为 .
查看习题详情和答案>>
| l | 3+ |
| g | 2+ |
| a | 2+ |
| e | 3+ |
| O | - 3 |
| O | 2- 3 |
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是
(2)为了确定X,观将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕灰色沉淀,向该沉淀中滴入稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解.则:
①X为
A.S
| O | 2- 3 |
| O | 2- 4 |
| O | 2- 3 |
②A中的化学键类型为
③B的水溶液中所有离子的浓度由大到小的顺序为
④将0.02mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为
⑤利用上述已经确定的物质,可以检验出D、E中的阳离子.请简述实验操作步骤、现象及结论:
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.则物质D一定含有上述离子中的