摘要:95.本题分子量用以下数据:H2O=18.0 CaO=56.0 CaO2=72.0 过氧化钙是一种安全无毒的氧化物.通常含有部分CaO.且带有数量不等的结晶水.为分析某过氧化物样品的组成.进行了如下实验. ①称取0.270克样品.灼热使之完全分解.生成CaO.O2和H2O.得到的O2在标准状况下的体积为33.6毫升. ②另取0.120克样品.溶于稀盐酸.加热煮沸使生成的H2O2完全分解.然后将溶液中的Ca2+完全转化成CaC2O4沉淀.经过滤洗涤后.将沉淀溶于热的稀硫酸.用0.0200摩/升KMnO4溶液滴定.共用去31.0毫升KMnO4溶液.化学方程式如下: 5CaC2O4+2KMnO4+8H2SO4=K2SO4+2MnSO4+5CaSO4+10CO2+8H2O (1)写出CaO2受热分解的化学方程式. (2)计算样品中的CaO2的质量分数. (3)计算样品中的CaO2·xH2O的x值. 答案:(1)2CaO2 = 2CaO+O2 (2)w(CaO2)=80% (3)x=0.5
网址:http://m.1010jiajiao.com/timu3_id_336969[举报]
(1997年全国,34)A、B都是芳香族化合物,1 mol A水解得到1 mol B和1 mol 醋酸。A、B式量都不超过200,完全燃烧含量为65.2%(即质量分数为0.652)。 A溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B式量之差为 。
(2)1个B分子中应该有 个氧原子。
(3)A的分子式是 。
(4)B可能有的三种结构简式是 、 、 。
查看习题详情和答案>>用质量分数为98%,密度为1.84g?cm-3的浓硫酸配制l mol/L稀硫酸100mL,其操作有以下各步:
①用量筒量取
②洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸转入100mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
(1)第①步操作中应用量筒量取
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是
(3)正确的操作顺序是(用序号填写)
(4)定容时,如果俯视刻度线,配制的硫酸浓度将偏
查看习题详情和答案>>
①用量筒量取
5.4
5.4
mL浓硫酸②洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸转入100mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
(1)第①步操作中应用量筒量取
5.4
5.4
mL浓硫酸;应选择10
10
mL量筒(填5、10或50).(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是
100mL容量瓶、胶头滴管
100mL容量瓶、胶头滴管
.(3)正确的操作顺序是(用序号填写)
①④③⑤②
①④③⑤②
.(4)定容时,如果俯视刻度线,配制的硫酸浓度将偏
大
大
(填大或小).若配制500mL 0.2mol/L的稀硫酸:
(1)需要量取质量分数为98%的硫酸(密度为1.84g?mL-1)
(2)下面是某学生的操作过程:
a.检查容量瓶是否漏水;b.用100mL的量筒量取浓硫酸;
c.将浓硫酸倒入另一个盛有适量蒸馏水的量筒中稀释,并冷却到室温;
d.用玻璃棒引流,将稀释后的硫酸倒入500mL的容量瓶;
e.轻轻摇动容量瓶,使瓶内液体混合均匀,再向容量瓶中加水至离刻度线1cm~2cm;
f.用胶头滴管加水至凹液面底部与刻度线相切,摇匀;
g.在容量瓶上贴上标签待用.
按照通常的配制要求,指出其中缺少或操作的错误,并补充或改正(有几项填几项,若空格不够可以补加).
①
(3)任何实验都有误差,在你改正后的操作中,产生误差的原因还有
(4)本实验最浪费时间的步骤是将稀释后的硫酸冷却到室温,为了节约时间,简便易行的加快稀硫酸冷却的方法是
查看习题详情和答案>>
(1)需要量取质量分数为98%的硫酸(密度为1.84g?mL-1)
5.4
5.4
mL.(2)下面是某学生的操作过程:
a.检查容量瓶是否漏水;b.用100mL的量筒量取浓硫酸;
c.将浓硫酸倒入另一个盛有适量蒸馏水的量筒中稀释,并冷却到室温;
d.用玻璃棒引流,将稀释后的硫酸倒入500mL的容量瓶;
e.轻轻摇动容量瓶,使瓶内液体混合均匀,再向容量瓶中加水至离刻度线1cm~2cm;
f.用胶头滴管加水至凹液面底部与刻度线相切,摇匀;
g.在容量瓶上贴上标签待用.
按照通常的配制要求,指出其中缺少或操作的错误,并补充或改正(有几项填几项,若空格不够可以补加).
①
缺少洗涤烧杯和玻璃棒的操作
缺少洗涤烧杯和玻璃棒的操作
;②量筒的规格错,应该用10mL的量筒量取浓H2SO4
量筒的规格错,应该用10mL的量筒量取浓H2SO4
;③不应该在量筒中稀释浓H2SO4,应用烧杯
不应该在量筒中稀释浓H2SO4,应用烧杯
;④不应该用容量瓶保存溶液,应用细口瓶
不应该用容量瓶保存溶液,应用细口瓶
;⑤无
无
.(3)任何实验都有误差,在你改正后的操作中,产生误差的原因还有
量筒的精确度不够高、读数误差、溶质仍有少量残留在烧杯内、室温未必是20℃等
量筒的精确度不够高、读数误差、溶质仍有少量残留在烧杯内、室温未必是20℃等
.(4)本实验最浪费时间的步骤是将稀释后的硫酸冷却到室温,为了节约时间,简便易行的加快稀硫酸冷却的方法是
充分搅拌或给盛有稀H2SO4的烧杯敷冰块
充分搅拌或给盛有稀H2SO4的烧杯敷冰块
.
在高一化学教材中,介绍了过氧化钠与二氧化碳及水的反应:
2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑
然而,过氧化钠与其他非金属氧化物(如:NO、NO2等)的反应能否发生呢?为此,某校化学兴趣小组设计了以下实验进行探究:
步骤一:NO、NO2的制备
①本实验所用的NO由饱和硫酸亚铁溶液与浓硫酸和粉末状硝酸钾反应制备,在酸性环境中硝酸根离子被还原为NO,得到的NO的纯度约为98%;
反应的化学方程式为:
②NO2由硝酸铅受热分解得到:2Pb(NO3)2=2PbO+4NO2↑+O2↑使生成的气体通过 (从以下选项中选择最佳方案)可以使NO2得以净化.
A.装有H2O的洗气瓶 B.置于冰水中的U形管(NO2沸点21℃)
C.装有浓硫酸的洗气瓶 D.装有Na2SO3溶液的洗气瓶
步骤二:操作(如图,b、c为弹簧夹)
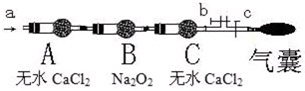
①先打开b关闭c,通入 (从所给选项选出)5分钟;目的是
A.空气 B.O2C.CO2 D.N2
②然后 ,再分别从a处通入NO或NO22分钟.
现象:当通入NO时,B中靠近A侧浅黄色固体变成黄色,气囊未见鼓起;当通入NO2时,B中靠近A侧浅黄色固体变成白色,气囊也未见鼓起;
步骤三:产物检验
分别取出B中黄色固体或白色固体进行检验,得知两种固体均为盐.
结论:
请写出NO2与 Na2O2反应的化学方程式: .
查看习题详情和答案>>
2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑
然而,过氧化钠与其他非金属氧化物(如:NO、NO2等)的反应能否发生呢?为此,某校化学兴趣小组设计了以下实验进行探究:
步骤一:NO、NO2的制备
①本实验所用的NO由饱和硫酸亚铁溶液与浓硫酸和粉末状硝酸钾反应制备,在酸性环境中硝酸根离子被还原为NO,得到的NO的纯度约为98%;
反应的化学方程式为:
②NO2由硝酸铅受热分解得到:2Pb(NO3)2=2PbO+4NO2↑+O2↑使生成的气体通过
A.装有H2O的洗气瓶 B.置于冰水中的U形管(NO2沸点21℃)
C.装有浓硫酸的洗气瓶 D.装有Na2SO3溶液的洗气瓶
步骤二:操作(如图,b、c为弹簧夹)

①先打开b关闭c,通入
A.空气 B.O2C.CO2 D.N2
②然后
现象:当通入NO时,B中靠近A侧浅黄色固体变成黄色,气囊未见鼓起;当通入NO2时,B中靠近A侧浅黄色固体变成白色,气囊也未见鼓起;
步骤三:产物检验
分别取出B中黄色固体或白色固体进行检验,得知两种固体均为盐.
结论:
请写出NO2与 Na2O2反应的化学方程式:
下表是稀硫酸与某金属反应的实验数据:
(1)实验4和5表明
(2)仅表明反应物浓度对反应速率产生影响的实验有:
(3)本实验中影响反应速率的其他因素还有
查看习题详情和答案>>
| 实验序号 |
金属 质量/g |
金属状态 |
c(H2SO4) /mol?L-1 |
V(H2SO4) /mL |
溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
6 6 |
0.10 0.10 |
丝 丝 |
1.0 1.0 |
50 50 |
20 20 |
35 35 |
125 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
固体反应物的表面积
固体反应物的表面积
对反应速率有影响,表面积越大
表面积越大
反应速率越快,能表明同一规律的实验还有1和2
1和2
(填实验序号);(2)仅表明反应物浓度对反应速率产生影响的实验有:
1、3、4、6、8或2、5
1、3、4、6、8或2、5
(填实验序号);(3)本实验中影响反应速率的其他因素还有
反应温度
反应温度
,其实验序号是6和7或8和9
6和7或8和9
.