摘要:67.NA代表阿伏加德罗常数.下列说法正确的是 C A.9gD2O中含有的电子数为5NA B.1molMgCl2中含有的离子数为2NA C.1molCH4分子中共价键总数为4NA D.7.1g C12与足量NaOH溶液反应转移的电子数为0.2NA
网址:http://m.1010jiajiao.com/timu3_id_336941[举报]
(2012?信阳一模)实验室有NH4HCO3和NaHSO3的干燥粉状混合物,某兴趣小组为测定其中NH4HCO3的含量,设计了用在混合物中加酸的实验方法来测定其质量分数.回答以下问题:
(1)化学小组主要选用了下列药品和仪器进行实验.(图中每种仪器装置只选用了一次,铁架台等固定仪器未画出)

请按气流由左向右的方向,仪器连接顺序是(填仪器的接口字母a、b…)
a→
(2)实验开始,混合物加酸前,A装置需要鼓入空气,作用是
(3)E装置的作用是
(4)实验中,若C瓶中溶液褪色,则测定结果可能会偏
mL.
(5)若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质量分数为
(6)从定量测定的准确性考虑,该套装置还应作进一步的改进是
可能用到的相对原子质量:H~1 C~12 N~14 O~16 Na~23 S~32.
查看习题详情和答案>>
(1)化学小组主要选用了下列药品和仪器进行实验.(图中每种仪器装置只选用了一次,铁架台等固定仪器未画出)

请按气流由左向右的方向,仪器连接顺序是(填仪器的接口字母a、b…)
a→
i
i
→h
h
→d
d
→e
e
→f→g→b
b
→c
c
.(2)实验开始,混合物加酸前,A装置需要鼓入空气,作用是
排出装置中原有空气
排出装置中原有空气
;加酸后A装置再次鼓入空气的作用是将生成的气体全部送入后续装置
将生成的气体全部送入后续装置
.(3)E装置的作用是
吸收二氧化硫气体,防止二氧化硫对测定结果的影响
吸收二氧化硫气体,防止二氧化硫对测定结果的影响
.(4)实验中,若C瓶中溶液褪色,则测定结果可能会偏
高
高
(填“高”或“低”).为了确保实验中C瓶溶液不褪色,若取样品的质量为m g,实验前 E中所装 a mol?L-1的KMnO4溶液体积(V)不少于| 50m |
| 13a |
| 50m |
| 13a |
(5)若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质量分数为
60.3%
60.3%
.(6)从定量测定的准确性考虑,该套装置还应作进一步的改进是
在B之后再接一个阻止空气中水和二氧化碳进入B的装置
在B之后再接一个阻止空气中水和二氧化碳进入B的装置
.可能用到的相对原子质量:H~1 C~12 N~14 O~16 Na~23 S~32.
图1是化学研究性学习小组设计的铜与稀硝酸反应的两个实验装置图.其中装置Ⅰ为甲同学设计.(可能用到的相对原子质量:H:1 C:12 N:14 O:16 Cu:64 )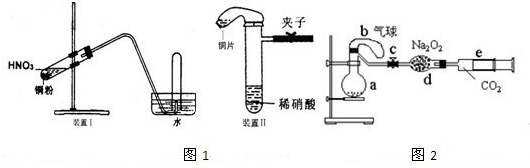
请回答下列问题:
(1)铜与稀硝酸反应的离子方程式为
(2)乙同学认为装置Ⅰ中收集的气体不能确定铜与稀硝酸反应生成的是NO气体,理由是
(3)化学研究性学习小组的其它同学对上述实验进行了研究,认为装置Ⅱ只能定性研究铜与硝酸的反应,他们又重新设计了一套实验,装置图如图2:a中盛有标况下的空气(氧气占五分之一)和10mL,1.2mol/L硝酸的250mL烧瓶.b是未充气(实验开始前内部没有气体)放有0.384g铜粉的气球.(整套装置已经过气密性检查合格.)他们做了以下实验,请填写有关空白:
①将气球中的铜粉小心倒入烧瓶中,充分反应后发现 铜粉有余(设产生的气体不溶解于溶液中),则可观察到的是
②将烧瓶不断振荡发现气球逐渐缩小,发生有关反应的化学方程式是:
③打开弹簧夹将二氧化碳慢慢推入干燥管内继续振荡,使气体与气体、溶液充分接触,欲使所有的铜粉都溶解,至少需要推入二氧化碳
④将上述全过程用一个总的化学方程式表示:
查看习题详情和答案>>

请回答下列问题:
(1)铜与稀硝酸反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(2)乙同学认为装置Ⅰ中收集的气体不能确定铜与稀硝酸反应生成的是NO气体,理由是
NO2与水反应也可产生NO:3NO2+H2O=2HNO3+NO,故不能肯定生成的NO气体是来自于铜与稀硝酸反应
NO2与水反应也可产生NO:3NO2+H2O=2HNO3+NO,故不能肯定生成的NO气体是来自于铜与稀硝酸反应
.于是他设计装置Ⅱ,其中装铜片的是气球.(3)化学研究性学习小组的其它同学对上述实验进行了研究,认为装置Ⅱ只能定性研究铜与硝酸的反应,他们又重新设计了一套实验,装置图如图2:a中盛有标况下的空气(氧气占五分之一)和10mL,1.2mol/L硝酸的250mL烧瓶.b是未充气(实验开始前内部没有气体)放有0.384g铜粉的气球.(整套装置已经过气密性检查合格.)他们做了以下实验,请填写有关空白:
①将气球中的铜粉小心倒入烧瓶中,充分反应后发现 铜粉有余(设产生的气体不溶解于溶液中),则可观察到的是
溶液变蓝色,烧瓶内气体由无色继而变成红色,气球胀大
溶液变蓝色,烧瓶内气体由无色继而变成红色,气球胀大
;②将烧瓶不断振荡发现气球逐渐缩小,发生有关反应的化学方程式是:
NO2+O2+2H2O═4HNO3、或4NO+3O2+2H2O═4HNO3
NO2+O2+2H2O═4HNO3、或4NO+3O2+2H2O═4HNO3
;③打开弹簧夹将二氧化碳慢慢推入干燥管内继续振荡,使气体与气体、溶液充分接触,欲使所有的铜粉都溶解,至少需要推入二氧化碳
38.4
38.4
ml;④将上述全过程用一个总的化学方程式表示:
2Cu+4HNO3+O2═2Cu(NO3)2+2H2O
2Cu+4HNO3+O2═2Cu(NO3)2+2H2O
.化学反应速率公式是由实验测定的.例如H2+Cl2=2HCl的速率公式可表示为:v=kcm(H2)cn(Cl2),式中k为反应速率常数,m和n的数值可以用下表的数据推算出:
由此推知,m和n的正确的值为( )
| c(H2)mol/L | c(Cl2)mol/L | v/mol/L?s |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
| A、m=1 n=1 | ||||
B、m=
| ||||
C、m=
| ||||
D、m=1 n=
|
在100℃时,将0.1mol的四氧化二氮气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下数据:
(1)该反应的化学方程式为
(2)20s时四氧化二氮的浓度C1=
查看习题详情和答案>>
| 浓度 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4)/mol?L-1 | 0.1 | c1 | 0.05 | C3 | a | b |
| C(NO2)/mol?L-1 | 0 | 0.06 | C2 | 0.12 | 0.12 | 0.12 |
N2O4=2NO2
N2O4=2NO2
,达到平衡时四氧化二氮的转化率为60
60
%,表中C2>
>
C3=
=
a=
=
b(选填“>”、“<”、“═”).(2)20s时四氧化二氮的浓度C1=
0.07
0.07
mol?l-1,在0s~20s内四氧化二氮的平均反应速率为0.0015
0.0015
mol?(L?s)-1.(16分)实验室有NH4HCO3和NaHSO3的干燥粉状混合物,某兴趣小组为测定其中NH4HCO3的含量,设计了用在混合物中加酸的实验方法来测定其质量分数。回答以下问题:
⑴化学小组主要选用了下列药品和仪器进行实验。(图中每种仪器装置只选用了一次,铁架台等固定仪器未画出)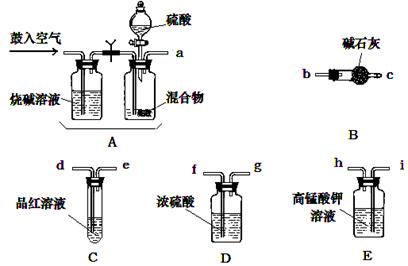
请按气流由左向右的方向,仪器连接顺序是(填仪器的接口字母a、b...)
a→ → → → → f →g → → 。
⑵实验开始,混合物加酸前,A装置需要鼓入空气,作用是 ;加酸后A装置再次鼓入空气的作用是 。
⑶ E装置的作用是 。
⑷实验中,若C瓶中溶液褪色,则测定结果可能会偏 (填“高”或“低”)。为了确
保实验中C瓶溶液不褪色,若取样品的质量为m g,实验前 E中所装 a mol·L-1的KMnO4
溶液体积(V)不少于 mL。
⑸若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质
量分数为 。
⑹从定量测定的准确性考虑,该套装置还应作进一步的改进是 。
可能用到的相对原子质量:H~1 C~12 N~14 O~16 Na~23 S~32