摘要:35.已知某盐在不同温度下的溶解度. 若把质量分数为22%的该盐溶液由60℃逐渐冷却.则开始析出晶体的温度应在 D A.0℃-10℃ B.10℃-20℃ C.20℃-30℃ D.30℃-40℃
网址:http://m.1010jiajiao.com/timu3_id_336909[举报]
(1999年上海,12)已知某盐在不同温度下的溶解度(见下表)
T(℃) | 0 | 10 | 20 | 30 | 40 |
S(克/100克水) | 11.5 | 15.1 | 19.4 | 24.4 | 37.6 |
若把质量分数为22%的该盐溶液由60℃逐渐冷却,则开始析出晶体的温度应( )
A.0℃~10℃ B.10℃~20℃ C.20℃~30℃ D.30℃~40℃
查看习题详情和答案>>
(1997年上海,12)你认为减少酸雨产生的途径可采取的措施是①用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源 ( )
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
查看习题详情和答案>>(2011?上海模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E是人体内含量最高的金属元素.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的非金属性由强到弱的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式
 ;一种由B、C组成的化合物与AC2电子数相等,其化学式为
;一种由B、C组成的化合物与AC2电子数相等,其化学式为
(4)E的核外电子排布式是
(5)10molB的最高价氧化物对应的水化物的稀溶液与4molD的单质反应时,B被还原到最低价,B被还原后的产物化学式为
查看习题详情和答案>>
(1)A、B、C的非金属性由强到弱的顺序为
O>N>C
O>N>C
.(2)B的氢化物的分子空间构型是
三角锥型
三角锥型
.它是极性分子
极性分子
(填极性和非极性)分子.(3)写出化合物AC2的电子式


N2O
N2O
.(4)E的核外电子排布式是
1s22s22p63s23p64s2
1s22s22p63s23p64s2
,(5)10molB的最高价氧化物对应的水化物的稀溶液与4molD的单质反应时,B被还原到最低价,B被还原后的产物化学式为
NH4NO3
NH4NO3
.
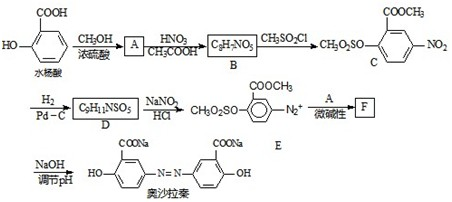
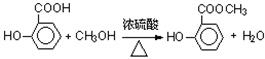
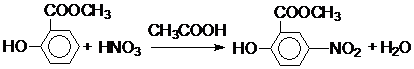
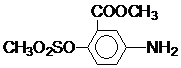
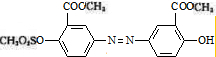
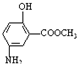 )也可用于合成奥沙拉秦.它的一种同分异构体X是α-氨基酸,能与FeCl3发生显色反应,其分子中共有6种化学环境不同的H原子.X的结构简式为
)也可用于合成奥沙拉秦.它的一种同分异构体X是α-氨基酸,能与FeCl3发生显色反应,其分子中共有6种化学环境不同的H原子.X的结构简式为