网址:http://m.1010jiajiao.com/timu3_id_335820[举报]
(Ⅰ)下列实验操作或对实验事实的描述正确的是 (填序号);
① 实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉。
② 配制一定浓度的溶液时,俯视容量瓶的刻度线,会使配制的浓度偏高;实验室测定中和热时,过早读数会使测定结果偏低。
③ 将Fe2(SO4)3溶液加热蒸发至干并灼烧,最后得到红棕色粉末
④ 实验室用铜片与稀硝酸反应产生的气体可用排水法收集
⑤ 试管中加入少量淀粉,再加入一定量稀硫酸,加热3-4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现
⑥ 向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水现象相同
⑦ 苯与溴水在铁粉的催化作用下制备溴苯
⑧ 分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积一样多
Ⅱ.在中学化学实验中,通常用无水硫酸铜来检验少量水的存在。由于无水硫酸铜吸湿性很强,需要现制现用。
方法甲:取2药匙细小的硫酸铜晶体置于_______中研碎后放入坩埚,将坩埚放在______上用小火慢慢加热并用玻璃棒不停搅拌,最后将坩埚移入___________中进行冷却(请选用合适仪器填空:表面皿、研钵、烧杯、通风橱、试管夹、干燥器、泥三角)。
方法乙:取2药匙研碎的硫酸铜晶体于小烧杯中,加入20 mL浓硫酸(质量分数不低于98%),并用玻璃棒搅拌,静置5 min后倾去浓硫酸,用无水乙醇洗涤数次,倒在滤纸上晾干。
【交流与讨论】
(1)方法甲中,加热温度稍高时会出现变黑现象,原因是_________(用化学方程式表示)。
(2)方法乙中,浓硫酸的作用是__________;为了不浪费药品,对无水乙醇洗涤液进行再生的方法是______ ,所用的主要玻璃仪器有烧瓶、接液管、锥形瓶、酒精灯________________等。
(3)用制得的无水硫酸铜检验某双氧水中是否含水时,除了发现固体变蓝外,还发现该双氧水中有气泡产生,对此你有何猜想______________。
 (4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。
(4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。
【问题一】如图装置中,分液漏斗内装的液体是________,反应结束时,获取CuSO4•5H2O的操作过程是先________________,趁热将三颈瓶中的液体倒入烧杯中冷却,析出晶体CuSO4?5H2O ,过滤、晾干。
【问题二】工业上用石灰乳吸收尾气,除了防止环境污染外,还能得到了有经济实用价值的副产品―― 亚硝酸钙。尾气吸收生成亚硝酸钙的化学方程式是_______________。
查看习题详情和答案>>①亚硫酸钠溶液中加入硝酸:S
| O | 2- 4 |
②澄清石灰水跟稀硝酸反应:Ca(OH)2+2H+?Ca2++2H2O
③向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全Ba(OH)2+2OH-+H++S
| O | 2- 4 |
| H | + 4 |
④0.1mol Br2中滴入含Cl2 0.1mol氯水:2Fe2++4Br-+3Cl2?2Fe3++2Br2+6Cl-
⑤向氢氧化钠溶液中加入少量碳酸氢钙溶液:Ca2++2HCO3-+2OH-?CaCO3 ↓+CO32-+2H2O
⑥硫化钠的水解:S2-+2H2O?H2S+2OH-
⑦向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++HC
| O | - 3 |
⑧某酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+C
| O | 2- 3 |
| A、③⑤ | B、①③ |
| C、③⑤⑥ | D、①②④⑥ |
下列有关反应的离子方程式书写正确的是
- A.亚硫酸氢铵溶液与含等物质的量的NaOH的溶液混合:
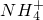 +
+ +2OH-
+2OH-
 +NH3↑+2H2O
+NH3↑+2H2O - B.氢氧化钡溶液与硫酸氢钠溶液反应至溶液恰好呈中性:Ba2++2H++
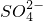 +2OH-
+2OH- BaSO4↓+2H2O
BaSO4↓+2H2O - C.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至
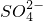 恰好沉淀完全:2Al3++3
恰好沉淀完全:2Al3++3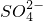 +3Ba2++6OH-
+3Ba2++6OH- 2Al(OH)3↓+3BaSO4↓
2Al(OH)3↓+3BaSO4↓ - D.向碳酸氢镁溶液中加入过量澄清石灰水:Mg2++
 +Ca2++2OH-
+Ca2++2OH- CaCO3↓+2H2O+MgCO3↓
CaCO3↓+2H2O+MgCO3↓