摘要:当锌与某浓度的硝酸反应时.若参加反应的锌与硝酸的物质的量之比为2:5.则硝酸的还原产物可能是┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈┈ A.N2O B.NO2 C.NO D.NH4NO3 出题背景:此题学生必须紧扣氧化还原反应中电子转移的实质去思考.硝酸变成其它含氮化合物时得电子数目必与锌失电子数目相等.同时必须明白参加反应的硝酸中既有被还原的.也有显酸性化合价不变的.2Zn – 2Zn2+ 失电子数:2 ×(2-0) 4HNO3 – 2Zn(NO3)2 HNO3 – 1NX+ 得电子数:1× = 1×(5-x) 解得:x = +1 相关试题:上海卷02年-考题22
网址:http://m.1010jiajiao.com/timu3_id_335426[举报]
当Zn与某浓度的硝酸反应时,若参加反应的锌与硝酸的物质的量之比为2∶5时,则还原产物可能是( )
①N2O ②NO ③NO2 ④N2O5 ⑤NH4NO3
A.①⑤ B.② C.④ D.②⑤
查看习题详情和答案>>|
当Zn与某浓度的硝酸反应时,若参加反应的锌与硝酸的物质的量之比为2∶5时,则还原产物可能是 ①N2O ②NO ③NO2 ④N2O5 ⑤NH4NO3 | |
| [ ] | |
A. |
①⑤ |
B. |
② |
C. |
④ |
D. |
②⑤ |
(11分)某研究性学习小组为探究铜、锌与浓盐酸的反应,设计实验探究方案如下:
实验用品:纯锌片、铜片、37%的浓盐酸、蒸馏水、氯化钾溶液、稀硝酸溶液
实验记录:
背影资料:
|
|
请你参与以下探究:
(1)实验A反应速度明显比B小,原因是 。
(2)根据“铜位于金属活动顺序表氢之后,与稀盐酸不反应,而在实验中加热时又产生气体”的事实,作出如下推断:
①有同学认为“实验C中加热时产生的气体是溶解在溶液中的H2”,你认为是否有道理,理由是 。
②某同学作了如下猜想:是否成立?请你设计实验方案加入验证。
| 猜想 | 验证方法 | 预测现象及结论 |
| 认为铜片中可能含有锌等杂质 | | |
| 猜想 | 预计验证方法 | 猜想的现象与结论 |
| 白色沉淀是氯化亚铜 | | |
| | |
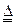 2Cu2O+O2↑
2Cu2O+O2↑