摘要:8下列各组热化学方程式中.化学反应的△H前者大于后者的是 ①C(s)+O2(g)====CO2(g),△H1 C(s)+O2,△H2 ②S(s)+O2(g)====SO2(g),△H3 S(g)+O2(g)====SO2(g),△H4 ③H2(g)+O2(g)===H2O(l),△H5 2H2(g)+O2(g)====2H2O(l),△H6 ④CaCO3+CO2(g),△H7 CaO(s)+H2O2(s),△H8 A.① B.④ C.②③④ D.①②③
网址:http://m.1010jiajiao.com/timu3_id_335289[举报]
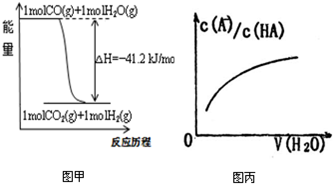
关于下列各图的叙述不正确的是( )
| 化学方程式 | 平衡常数K |
| F2+H22HF | 6.5×1095 |
| Cl2+H22HCl | 2.6×1033 |
| Br2+H22HBr | 1.9×1019 |
| I2+H22HI | 8.7×102 |

| A、已知CO的燃烧热283kJ/mol,2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol,则图甲表示CO和H2O(g)生成CO2和H2的能量变化 | ||
| B、某温度下,pH=11的NH3?H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3?H2O与NH3三种微粒的平衡浓度之和为0.05mol?Lˉ1 | ||
| C、在常温下,X2(g)和H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱 | ||
D、图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
|
Ⅰ.已知氢氟酸、醋酸、氢氰酸(HCN)、碳酸在室温下的电离常数分别为:
根据上述数据,回答下列问题:
(1)四种酸中酸性最强的是
(2)写出H2CO3电离方程式是
(3)写出下列反应的化学方程式:足量的氢氟酸与碳酸钠溶液混合:
Ⅱ.氨水中存在:NH3?H2O?NH4++OH-,在5份0.01mol?L-1的氨水中分别加入下列各物质:
A.浓氨水 B.纯水 C.少量NaOH固体 D.少量浓硫酸 E.NH4Cl固体
按照要求填空:
(1)电离平衡会向正向移动是
(2)c(NH4+)、c(OH-)都增大的是
(3)c(NH4+)增大,c(OH-)减小的是
查看习题详情和答案>>
| ① | HF | Ka=6.8×10-4 mol?L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol?L-1 |
| ③ | HCN | Ka=6.2×10-10 mol?L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7mol?L-1 Ka2=4.7×10-11 mol?L-1 |
(1)四种酸中酸性最强的是
HF
HF
,四种酸中酸性最弱的是HCN
HCN
.(2)写出H2CO3电离方程式是
H2CO3?HCO3-+H+
H2CO3?HCO3-+H+
、HCO3-?CO32-+H+
HCO3-?CO32-+H+
.(3)写出下列反应的化学方程式:足量的氢氟酸与碳酸钠溶液混合:
2HF+Na2CO3═2NaF+H2O+CO2↑
2HF+Na2CO3═2NaF+H2O+CO2↑
;足量的CO2通入NaCN溶液中:NaCN+H2O+CO2═HCN+NaHCO3
NaCN+H2O+CO2═HCN+NaHCO3
.Ⅱ.氨水中存在:NH3?H2O?NH4++OH-,在5份0.01mol?L-1的氨水中分别加入下列各物质:
A.浓氨水 B.纯水 C.少量NaOH固体 D.少量浓硫酸 E.NH4Cl固体
按照要求填空:
(1)电离平衡会向正向移动是
ABD
ABD
;电离平衡会向逆向移动是CE
CE
.(2)c(NH4+)、c(OH-)都增大的是
A
A
;c(NH4+)、c(OH-)都较小的是B
B
.(3)c(NH4+)增大,c(OH-)减小的是
E
E
;c(NH4+)减小,c(OH-)增大的是C
C
.