摘要:15.在60 oC恒温条件下.将含溶质A的某溶液200g分成甲.乙两等分.甲蒸发掉10g水后.析出5g A的无水晶体.乙蒸发掉20g水后.析出的15gA的无水晶体.则A在60oC时的溶解度为( ) A.50g B.100g C.150g D.200g
网址:http://m.1010jiajiao.com/timu3_id_334209[举报]
在恒容恒温条件下,能使可逆反应A(g)+B(g)==C(g)+D(g)正反应速率
增大的措施是 (g表示气体状态) ( )
A. 减少C或D的浓度 B. 增大D的浓度
C. 减少B的浓度 D. 增大A或B的浓度
查看习题详情和答案>>高铁酸钾(K2FeO4)具有极高的氧化性,且其还原产物为铁锈,对环境无不良影响.因该物质具有“绿色”、选择性高、活性强等特点受到人们关注.
I、高铁酸钾制备方法之一为:①在一定温度下,将氯气通入KOH溶液中制得次氯酸钾溶液;②在剧烈搅拌条件下,将Fe(NO3)3分批加入次氯酸钾溶液中,控制反应温度,以免次氯酸钾分解;③加 KOH至饱和,使K2FeO4 充分析出,再经纯化得产品,其纯度在95%以上.
(1)氯碱工业中制备氯气的化学方程式是 ;
(2)温度过高会导致次氯酸钾分解生成两种化合物,产物之一是氯酸钾(KClO3),另一种产物应该是 (写化学式)
(3)制备过程有一步反应如下,请配平此方程式(将计量数填入方框中):
Fe(OH)3+ ClO-+ OH-═ Fe
+ Cl-+ H2O
Ⅱ、为探究高铁酸钾的某种性质,进行如下两个实验:
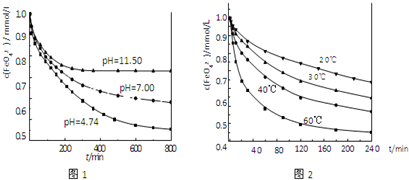
实验1:将适量K2FeO4分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0mmol?L-1(1mmol?L-1=10-3mol?L-1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800min后,三种溶液中高铁酸钾的浓度不再改变).
实验2:将适量 K2FeO4 溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0mmol?L-1 的试样,将试样分别置于 20℃、30℃、40℃和 60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2.
(4)实验1的目的是 ;
(5)实验2可得出的结论是 ;
(6)高铁酸钾在水中的反应为4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.
由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 ;
Ⅲ、高铁酸钾还是高能电池的电极材料.例如,Al-K2FeO4电池就是一种高能电池(以氢氧化钾溶液为电解质溶液),该电池放电时负极反应式是 .
查看习题详情和答案>>
I、高铁酸钾制备方法之一为:①在一定温度下,将氯气通入KOH溶液中制得次氯酸钾溶液;②在剧烈搅拌条件下,将Fe(NO3)3分批加入次氯酸钾溶液中,控制反应温度,以免次氯酸钾分解;③加 KOH至饱和,使K2FeO4 充分析出,再经纯化得产品,其纯度在95%以上.
(1)氯碱工业中制备氯气的化学方程式是
(2)温度过高会导致次氯酸钾分解生成两种化合物,产物之一是氯酸钾(KClO3),另一种产物应该是
(3)制备过程有一步反应如下,请配平此方程式(将计量数填入方框中):
| O | 2- 4 |
Ⅱ、为探究高铁酸钾的某种性质,进行如下两个实验:

实验1:将适量K2FeO4分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0mmol?L-1(1mmol?L-1=10-3mol?L-1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800min后,三种溶液中高铁酸钾的浓度不再改变).
实验2:将适量 K2FeO4 溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0mmol?L-1 的试样,将试样分别置于 20℃、30℃、40℃和 60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2.
(4)实验1的目的是
(5)实验2可得出的结论是
(6)高铁酸钾在水中的反应为4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.
由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
Ⅲ、高铁酸钾还是高能电池的电极材料.例如,Al-K2FeO4电池就是一种高能电池(以氢氧化钾溶液为电解质溶液),该电池放电时负极反应式是
高铁酸钾(K2FeO4)具有极高的氧化性,对环境无不良影响,被人们称为“绿色化学”试剂.某校化学兴趣小组对高铁酸钾进行了如下探究.
I、高铁酸钾制备:
①在一定温度下,将氯气通入KOH溶液中制得次氯酸钾溶液;②在剧烈搅拌条件下,将Fe(NO3)3 分批加入次氯酸钾溶液中,控制反应温度,以免次氯酸钾分解;③加 KOH至饱和,使K2FeO4 充分析出,再经纯化得产品.
(1)温度过高会导致次氯酸钾分解生成两种化合物,产物之一是氯酸钾(KClO3),此反应化学方程式是
(2)制备过程的主反应为(a、b、c、d、e、f为化学计量系数):aFe (OH) 3+b ClO-+cOH-=d FeO42-+e Cl-+f H2O,则a:f=
II、探究高铁酸钾的某种性质:
实验1:将适量K2FeO4分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0mmol?L-1(1mmol?L-1=10-3mol?L-1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800min后,三种溶液中高铁酸钾的浓度不再改变).
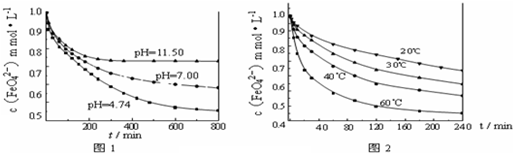
实验2:将适量 K2FeO4 溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0mmol?L-1 的试样,将试样分别置于 20℃、30℃、40℃和 60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2.
(3)实验1的目的是
(4)实验2可得出的结论是
(5)高铁酸钾在水中的反应为4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.
由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
Ⅲ、用高铁酸钾作高能电池的电极材料:
Al-K2FeO4电池是一种高能电池(以氢氧化钾为电解质溶液),该电池放电时负极反应式是:
查看习题详情和答案>>
I、高铁酸钾制备:
①在一定温度下,将氯气通入KOH溶液中制得次氯酸钾溶液;②在剧烈搅拌条件下,将Fe(NO3)3 分批加入次氯酸钾溶液中,控制反应温度,以免次氯酸钾分解;③加 KOH至饱和,使K2FeO4 充分析出,再经纯化得产品.
(1)温度过高会导致次氯酸钾分解生成两种化合物,产物之一是氯酸钾(KClO3),此反应化学方程式是
3KClO=KClO3+2KCl
3KClO=KClO3+2KCl
.(2)制备过程的主反应为(a、b、c、d、e、f为化学计量系数):aFe (OH) 3+b ClO-+cOH-=d FeO42-+e Cl-+f H2O,则a:f=
2:5
2:5
.II、探究高铁酸钾的某种性质:
实验1:将适量K2FeO4分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0mmol?L-1(1mmol?L-1=10-3mol?L-1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800min后,三种溶液中高铁酸钾的浓度不再改变).

实验2:将适量 K2FeO4 溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0mmol?L-1 的试样,将试样分别置于 20℃、30℃、40℃和 60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2.
(3)实验1的目的是
探究高铁酸钾在不同pH溶液中的稳定性(或与水反应的速率)
探究高铁酸钾在不同pH溶液中的稳定性(或与水反应的速率)
;(4)实验2可得出的结论是
温度越高,高铁酸钾越不稳定(或温度越高,高铁酸钾与水反应的速率越快)
温度越高,高铁酸钾越不稳定(或温度越高,高铁酸钾与水反应的速率越快)
;(5)高铁酸钾在水中的反应为4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.
由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
PH=11.50的溶液中OH-离子浓度大,使上述平衡向左移动
PH=11.50的溶液中OH-离子浓度大,使上述平衡向左移动
;Ⅲ、用高铁酸钾作高能电池的电极材料:
Al-K2FeO4电池是一种高能电池(以氢氧化钾为电解质溶液),该电池放电时负极反应式是:
Al-3e-+4OH-=AlO2-+2H2O
Al-3e-+4OH-=AlO2-+2H2O
.(1)在100℃恒温条件下将0.100mol的N2O4充入体积为1L的真空密闭容器中,发生反应:N2O4(g)?2NO2(g) H>0.隔一定时间对该容器内的物质进行分析,得到如下数据:
请回答下列问题:
①表中a=
②已知100℃时该反应的平衡常数为0.36,则表中b、c1、c2的大小关系为
,达到平衡时N2O4的转化率为
(2)室温下,把SiO2细粉放入蒸馏水中,不断搅拌,能形成H2SiO4溶液,反应原理如下:SiO2(s)+2H2O(l)?H2SiO4(aq)△H
①写出该反应的化学平衡常数K的表达式:
②实际上,在地球的深处,由于压强很大,固体、液体都会受到影响.在一定温度下,在10000m以下的地球深处,上述反应的方向是
查看习题详情和答案>>
 |
0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol?L-1 | 0.100 | a | 0.5b | 0.4b | ||
| c(NO2)/mol?L-1 | 0 | 0.060 | b | c1 | c2 | c3 |
①表中a=
0.070
0.070
,在0~20s内N2O4的平均反应速率为0.0015
0.0015
mol?(L?s)-1.②已知100℃时该反应的平衡常数为0.36,则表中b、c1、c2的大小关系为
b<c1=c2
b<c1=c2
,c3=0.120
0.120
mol?L-1 ,达到平衡时N2O4的转化率为
60%
60%
.(2)室温下,把SiO2细粉放入蒸馏水中,不断搅拌,能形成H2SiO4溶液,反应原理如下:SiO2(s)+2H2O(l)?H2SiO4(aq)△H
①写出该反应的化学平衡常数K的表达式:
K=c(H2SiO4)
K=c(H2SiO4)
.②实际上,在地球的深处,由于压强很大,固体、液体都会受到影响.在一定温度下,在10000m以下的地球深处,上述反应的方向是
正方向
正方向
(填“正方向”、“逆方向”或“不移动”),理由是由于固体和液体对会受到大压强的影响,所以K=
,增大压强平衡向正反应方向移动
| c(H2SiO4) |
| c(SiO2).c2(H2O) |
由于固体和液体对会受到大压强的影响,所以K=
,增大压强平衡向正反应方向移动
.| c(H2SiO4) |
| c(SiO2).c2(H2O) |
将1 mol I2(g)和2 mol H2置于某![]() 2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。
2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。

(1)达到平衡时,I2(g)的物质的量浓度为______________mol·L-1。
(2)若改变反应条件,在甲条件下w(HI)的变化如图曲线(Ⅱ)所示,在乙条件下w(HI)的变化如图曲线(Ⅲ)所示。则甲条件可能是______________,乙条件可能是______________。(填入下列条件的序号)
①恒容条件下,升高温度 ②恒容条件下,降低温度 ③恒温条件下,缩小反应容器体积 ④恒温条件下,扩大反应容器体积 ⑤恒温恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的