摘要:如图所示.在一两边有壁板.长为L=1m的水平 绝缘槽中.有水平向右的匀强电场.电场强度E=1.0× 103V/m.槽中有一质量m=0.1kg.带负电荷q=2×10-4 C的带电体.以水平初速v0=1m/s从槽 的左端向右滑动.已知带电体与水平绝缘槽的动摩擦因 数为μ=0.2.若带电体与竖直壁的碰撞过程中机械能不 损失.电量也不会改变.那么带电体在停下来之前.所通过的总路程是多少(取g=10m/s2)
网址:http://m.1010jiajiao.com/timu3_id_334056[举报]
Ⅰ。(每空1分,共4分)⑴通常状况下,甲同学取1 mol H2O加热到100℃时,液态水会汽化为水蒸气(如图所示),该过程属于 变化。
在保持压强不变的情况下,水蒸气的体积 
(填“>”、“<”或“=”)22.4L。
⑵乙同学做H2在O2中燃烧的实验,该实验过程属于 变化,在该变化过程中,一定保持相等的是 (填序号)。
| A.反应物分子数目与生成物分子数目 | B.反应物原子总物质的量与生成物原子总物质的量 |
| C.反应物总质量与生成物总质量 | D.反应物体积与生成物体积 |

⑴请写出下列仪器的名称: A ,B ,C 。
⑵仪器B上标记有 (填序号)。
①质量 ②温度
 ③刻度线 ④浓度 ⑤容积
③刻度线 ④浓度 ⑤容积⑶检验仪器B是否漏水的方法是 查看习题详情和答案>>
全世界每年被腐蚀损耗的钢铁约占全年钢铁产量的
,而在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因.
(1)在潮湿空气中,钢铁发生吸氧腐蚀转化为Fe(OH)2的电池反应方程式为
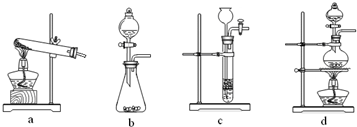
(2)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4
CO↑+CO2↑+H2O,下列装置中,可用作草酸分解制取气体的是
(3)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3?nH2O和Fe两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如图所示.

①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是
②在点燃酒精灯之前应进行的操作是:(a)检查装置气密性;(b)
③准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=
④在本实验中,下列情况会使测定结果n偏大的是
a.缺少洗气瓶B b.缺少装置E c.反应后固体是铁和少量Fe2O3?nH2O.
查看习题详情和答案>>
| 1 |
| 10 |
(1)在潮湿空气中,钢铁发生吸氧腐蚀转化为Fe(OH)2的电池反应方程式为
2Fe+O2+2H2O=2Fe(OH)2
2Fe+O2+2H2O=2Fe(OH)2
.
(2)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4
| 浓硫酸 |
| 加热 |
d
d
.(填字母)(3)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3?nH2O和Fe两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如图所示.

①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是
浓NaOH溶液
浓NaOH溶液
、浓硫酸
浓硫酸
.②在点燃酒精灯之前应进行的操作是:(a)检查装置气密性;(b)
通入混合气体一段时间
通入混合气体一段时间
.③准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=
2
2
.④在本实验中,下列情况会使测定结果n偏大的是
a
a
.(填字母)a.缺少洗气瓶B b.缺少装置E c.反应后固体是铁和少量Fe2O3?nH2O.
 有机物A是有机合成的中间体,分子中含2个氧原子,其燃烧产物n(CO2):n(H2O)=2:1,质谱图表明A的相对分子质量为188,在一定条件下可以转变为B和C(分子式:C4H6O),相关转化关系如图所示:
有机物A是有机合成的中间体,分子中含2个氧原子,其燃烧产物n(CO2):n(H2O)=2:1,质谱图表明A的相对分子质量为188,在一定条件下可以转变为B和C(分子式:C4H6O),相关转化关系如图所示:已知:①R-CH=CH-OH会自动转化为R-CH2-CHO;
②同一个碳原子上连有两个双键的结构不稳定;
③B苯环上的一氯取代物有两种同分异构体;C分子中无支链.
请根据以上信息,回答下列问题:
(1)A的分子式是
C12H12O2
C12H12O2
;(2)B中含氧官能团的名称是
羧基
羧基
;(3)F的结构简式是


(4)写出由C生成D的化学方程式:
CH2=CHCH2CHO+2Cu(OH)2
CH2=CHCH2COOH+Cu2O+2H2O
| △ |
CH2=CHCH2CHO+2Cu(OH)2
CH2=CHCH2COOH+Cu2O+2H2O
;| △ |
(5)C有多种同分异构体,其中与C具有相同官能团的同分异构体(不含C)共有
2
2
种;(6)上述转化过程中不涉及的有机反应类型有
③⑤
③⑤
(填序号).①取代反应 ②聚合反应 ③消去反应 ④氧化反应 ⑤还原反应 ⑥水解反应.
C60、金刚石和石墨的结构模型如图所示(石墨仅表示出其中的一层结构):

(1)C60、金刚石和石墨三者的关系是互为
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于
(3)硅晶体的结构跟金刚石相似,1mol硅晶体中含有硅硅单键的数目约是
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是
查看习题详情和答案>>

(1)C60、金刚石和石墨三者的关系是互为
B
B
;A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于
分子
分子
(填“离子”、“原子”或“分子”)晶体;(3)硅晶体的结构跟金刚石相似,1mol硅晶体中含有硅硅单键的数目约是
2
2
NA个;(4)石墨层状结构中,平均每个正六边形占有的碳原子数是
2
2
.(2011?下城区模拟)乙酰乙酸乙酯(CH3COCH2COOC2H5)是一种不溶于水的液体,熔点:-45°C,沸点:180.8℃,它是有机合成中常用的原料.在实验室,它可以由乙酸乙酯在乙醇钠的催化作用下缩合而制得,反应式为:
2CH3COOC2H5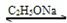 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH
反应中催化剂乙醇钠是由金属钠和残留在乙酸乙酯中的微量乙醇作用生成的,而一旦反应开始,生成的乙醇又会继续和钠反应生成乙酸钠.乙酰乙酸乙酯制备的流程如下:
金属钠,有机液体
钠熔化
小米状钠珠
橘红色溶液
含乙酰乙酸乙酯的混合物
乙酰乙酸乙酯粗产品
阅读下面关于乙酰乙酸乙酯制备的实验过程,并回答有关问题.
(1)将适量干净的金属钠放入烧瓶中,为了得到小米状的钠珠,需将钠熔化,为了防止钠的氧化,熔化时需在钠上覆盖一层有机液体,下表是钠和一些常用有机液体的物理性质:
最好选用
理由是
(2)将烧瓶中的有机液体小心倾出,迅速加入适量乙酸乙酯,装上带有一根长玻璃导管的单孔胶塞,并在导管上端接一个干燥管.缓缓加热,保持瓶中混合液微沸状态.在实验中,使用烧瓶必须干燥,原料乙酸乙酯必须无水,原因是
烧瓶配上长导管的作用是
(3)步骤⑥为向混合溶液中加入饱和食盐水,其目的是
粗产品(含乙酸乙酯和少量水及乙酸等)经过几步操作,最后成为纯品.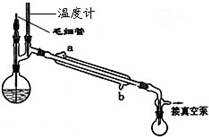
粗产品
乙酰乙酸乙酯
(4)向分离出的乙酰乙酸乙酯粗产品中加无水硫酸钠固体的作用是
(5)精馏乙酰乙酸乙酯时需要减压蒸馏,装置如图所示.
冷凝管的进出水方向应
(6)实验最后所得产品远少于完全转化的理论产值,除了反应过程中的损耗外,主要原因是
查看习题详情和答案>>
2CH3COOC2H5
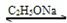 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH反应中催化剂乙醇钠是由金属钠和残留在乙酸乙酯中的微量乙醇作用生成的,而一旦反应开始,生成的乙醇又会继续和钠反应生成乙酸钠.乙酰乙酸乙酯制备的流程如下:
金属钠,有机液体
| 回流 |
| 振荡② |
| 回收有机液体③ |
| 加入乙酸乙酯④ |
| 乙酸酸化⑤ |
| ⑥ |
| ⑦ |
阅读下面关于乙酰乙酸乙酯制备的实验过程,并回答有关问题.
(1)将适量干净的金属钠放入烧瓶中,为了得到小米状的钠珠,需将钠熔化,为了防止钠的氧化,熔化时需在钠上覆盖一层有机液体,下表是钠和一些常用有机液体的物理性质:
| 钠 | 苯 | 甲苯 | 对二甲苯 | 四氯化碳 | |
| 密度(g/cm3) | 0.97 | 0.88 | 0.87 | 0.86 | 1.60 |
| 熔点(℃) | 97.8 | 5.5 | -95 | 13.3 | -22.8 |
| 沸点(℃) | 881.4 | 80 | 111 | 138.4 | 76.8 |
对二甲苯
对二甲苯
来熔化钠.是否能用四氯化碳?否
否
(填“是”或“否”)理由是
四氯化碳的沸点比钠的熔点低
四氯化碳的沸点比钠的熔点低
.(2)将烧瓶中的有机液体小心倾出,迅速加入适量乙酸乙酯,装上带有一根长玻璃导管的单孔胶塞,并在导管上端接一个干燥管.缓缓加热,保持瓶中混合液微沸状态.在实验中,使用烧瓶必须干燥,原料乙酸乙酯必须无水,原因是
有水则钠和水反应生成NaOH,使乙酸乙酯水解
有水则钠和水反应生成NaOH,使乙酸乙酯水解
,烧瓶配上长导管的作用是
导气及冷凝回流
导气及冷凝回流
,导管上端接一干燥管的目的是防止空气中的水蒸气进入烧瓶
防止空气中的水蒸气进入烧瓶
.(3)步骤⑥为向混合溶液中加入饱和食盐水,其目的是
使乙酰乙酸乙酯分层析出(分层)
使乙酰乙酸乙酯分层析出(分层)
,写出步骤⑦实验操作的主要仪器分液漏斗
分液漏斗
(填最主要一种).粗产品(含乙酸乙酯和少量水及乙酸等)经过几步操作,最后成为纯品.

粗产品
| 无水硫酸钠 |
| 过滤 |
| 水浴蒸馏 |
| 减压蒸馏 |
(4)向分离出的乙酰乙酸乙酯粗产品中加无水硫酸钠固体的作用是
干燥水分
干燥水分
.(5)精馏乙酰乙酸乙酯时需要减压蒸馏,装置如图所示.
冷凝管的进出水方向应
b
b
口进,a
a
口出.毛细管的作用是平衡压强、提供汽化中心、防暴沸
平衡压强、提供汽化中心、防暴沸
.(6)实验最后所得产品远少于完全转化的理论产值,除了反应过程中的损耗外,主要原因是
反应是可逆反应,只能部分转化
反应是可逆反应,只能部分转化
.