网址:http://m.1010jiajiao.com/timu3_id_333297[举报]
(18分)在容积不同的多个密闭容器内,分别充入同量的N2和H2,在不同温度下,同时发生反应N2+3H2 2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:
2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:
(1)A,B,C,D,E五点中,尚未达到化学平衡状态的点是 。
(2) 向一恒容容器中加入1 mol N2 和3 mol H2,T3时,测得体系压强为原来的7/8,并放出23.1 kJ的热量,则该反应的热化学方程式为 。
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3产率的有 (填字母)
| A.升高温度 | B.降低温度 | C.增大压强 | D.减小压强 |
(4)AC段的曲线和CE段曲线变化趋势相反,试从反应速率和平衡角度说明理由。
。 查看习题详情和答案>>
(18分)在容积不同的多个密闭容器内,分别充入同量的N2和H2,在不同温度下,同时发生反应N2+3H2 2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:
2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:

(1)A,B,C,D,E五点中,尚未达到化学平衡状态的点是 。
(2) 向一恒容容器中加入1 mol N2 和3 mol H2,T3时,测得体系压强为原来的7/8,并放出23.1 kJ的热量,则该反应的热化学方程式为 。
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3产率的有 (填字母)
A.升高温度 B.降低温度 C.增大压强 D.减小压强
E.加入催化剂 F.吸收NH3 G.通入N2
(4)AC段的曲线和CE段曲线变化趋势相反,试从反应速率和平衡角度说明理由。
。
查看习题详情和答案>>

请回答下列问题:
(1)简述乙烯的一种重要工业用途:___________________________________________。
(2)实验室制取乙烯的化学方程式为__________________________________。
(3)D的结构简式为__________________________________。
(4)I(C6H10O4)有多种同分异构体,其中符合HOOC—COOC4H9的同分异构体共有______________种。
(5)写出下列转化的化学方程式并指出指定反应的反应类型。
E![]() F:__________________________________。
F:__________________________________。
G+H![]() I:___________________________,反应类型:_________________。
I:___________________________,反应类型:_________________。
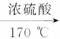
请回答下列问题:
(1)简述乙烯的一种重要工业用途:_____________________。
(2)实验室制取乙烯的化学方程式为________________________。
(3)D的结构简式为__________________。
(4)I(C6H10O4)有多种同分异构体,其中符合HOOC—COOC4H9的同分异构体共有___________种。
(5)写出下列转化的化学方程式并指出指定反应的反应类型。
E![]() F:__________________________。
F:__________________________。
G+H![]() I:___________________,反应类型:_________________________。
I:___________________,反应类型:_________________________。
| 熔点 ℃ |
沸点 ℃ |
液态时 密度 g/cm3 |
18℃时在水中的溶解度 mL/L |
乙醚、丙酮 或苯中的 溶解性 |
乙醇 中的 溶解性 |
| -97.73 | -24.2 | 0.9159 | 280 | 互溶 | 能溶 |

制备装置的分液漏斗中盛有甲醇,烧瓶中盛有浓盐酸.
请填写下列空白:
(1)制备一氯甲烷的化学方程式是
(2)装置e中可能发生反应的化学方程式是
(3)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃的燃烧现象有明显区别,且生成物中有HCl).CH3Cl燃烧的化学方程式是
(4)装置b的作用是