摘要:用r表示两个分子间的距离.Ep表示两个分子间相互作用的势能.当r=r0时.两分子间斥力等于引力.设两分子相距很远时Ep= 0.则: ①当r>r0时.由于分子斥力做正功.所以Ep随r的增大而减小 ②当r<r0时.由于分子斥力做负功.所以Ep随r的减小而增加 ③当r=r0时.Ep的值最大 ④当r=r0时.Ep的值为零 以上说法正确的是 A.①② B.①②④ C.② D.①②③
网址:http://m.1010jiajiao.com/timu3_id_333288[举报]
已知A、B、C、D、E、F都是周期表中前四周期的元素.它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出C原子的价层电子排布图
 ,F位于周期表
,F位于周期表
(2)A、B、C的第一电离能由小到大的顺序为
(3)F和质子数为25的M的部分电离能数据列于下表
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是
(4)晶胞中F原子的配位数为
g/cm3
g/cm3(用含r的表达式表示),该晶胞中原子空间利用率为
(5)H2S和C元素的氢化物(分子式为H2C2的主要物理性质比较如下
H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因
查看习题详情和答案>>
(1)写出C原子的价层电子排布图


d
d
区.(2)A、B、C的第一电离能由小到大的顺序为
C<O<N
C<O<N
.(写元素符号)(3)F和质子数为25的M的部分电离能数据列于下表
| 元素 | M | F | |
| 电离能(kJ?mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
Mn2+的3d轨道电子排布为半满状态较稳定
Mn2+的3d轨道电子排布为半满状态较稳定
.(4)晶胞中F原子的配位数为
8
8
,若F原子的半径为rcm,则F晶体的密度为| 112 | ||||
6.02×1023×(
|
| 112 | ||||
6.02×1023×(
|
68%
68%
.(5)H2S和C元素的氢化物(分子式为H2C2的主要物理性质比较如下
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 比任意比互溶 |
H2O2分子间存在氢键,与水分子可形成氢键
H2O2分子间存在氢键,与水分子可形成氢键
.[选修-物质结构与性质]
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.
请回答下列问题:
(1)A元素形成的晶体属于A2密堆积型式,则其晶体内晶胞类型应属于
(填写“六方”、“面心立方”或“体心立方”).
(2)B-的电子排布式为
(3)C的氢化物的空间构型为
(4)B元素的电负性
(5)如图所示是R形成的晶体的晶胞,设晶胞的棱长为a cm.试计算R晶体的密度为
g?cm-3
g?cm-3.(阿伏加德罗常数用NA表示)

查看习题详情和答案>>
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.
请回答下列问题:
(1)A元素形成的晶体属于A2密堆积型式,则其晶体内晶胞类型应属于
体心立方
体心立方
(填写“六方”、“面心立方”或“体心立方”).
(2)B-的电子排布式为
ls22s22p63s23p6
ls22s22p63s23p6
,在CB3分子中C元素原子的原子轨道发生的是sp3
sp3
杂化.(3)C的氢化物的空间构型为
三角锥形
三角锥形
,其氢化物在同族元素所形成的氢化物中沸点最高的原因是氨分子间形成氢键,所以氨气比同族其它元素形成的氢化物沸点高
氨分子间形成氢键,所以氨气比同族其它元素形成的氢化物沸点高
.(4)B元素的电负性
>
>
D元素的电负性(填“>”、“<”或“=”);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:H2S+Cl2=2HCl+S↓
H2S+Cl2=2HCl+S↓
.(5)如图所示是R形成的晶体的晶胞,设晶胞的棱长为a cm.试计算R晶体的密度为
| 312 |
| a3NA |
| 312 |
| a3NA |

【化学--选修3物质结构与性质】
W、Y、Z、Q、R是周期表中前四周期的元素,且原子序数依次增大.W原子核外有2个未成对电子,Q是电负性最大的元素,R元素的原子核外的未成对电子数是W原子核外未成对电子数的2倍.请回答下列问题(答题时,W、Y、Z、Q、R用所对应的元素符号表示):
(l)W、Y、Z 三种元素的第一电离能由大到小的顺序为 .在上述三种元素的原子中,写出与WZ2互为等电子体的分子式 .
(2)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键)
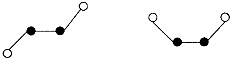
该分子中Y原子的杂化方式是 杂化.
(3)W2-2阴离子的电子式为 ,Z原子最外层电子排布式为 .
(4)YQ3分子的空间构型为 ,Y和Q两元素的氢化物的沸点相比较,高者是 (写分子式).往硫酸铜溶液中通入过量的YH3(Y的氢化物分子式),可生成配离子[Cu(YH3)4]2+,但YQ3不易与Cu2+形成配离子,其原因是 .
(5)科学家通过X射线探明RZ的晶体结构与NaCl晶体结构相似.那么在RZ晶体中距离R2+最近且等距离的R2+有 个.若在RZ晶体中阴阳离子间最近距离为a cm,晶体密度为ρg/cm3,则阿伏伽德罗常数NA的表达式为 mol-1.
(6)已知非整数比化合物R0.95Z,其晶体结构与NaCI相似,但由于R、Z离子个数比小于1:1,故晶体存在缺陷.R0.95Z可表示为
A、R
R
Z B、R
R
Z C、R
R
Z D、Fe2+0.85Fe3+0.1O.
查看习题详情和答案>>
W、Y、Z、Q、R是周期表中前四周期的元素,且原子序数依次增大.W原子核外有2个未成对电子,Q是电负性最大的元素,R元素的原子核外的未成对电子数是W原子核外未成对电子数的2倍.请回答下列问题(答题时,W、Y、Z、Q、R用所对应的元素符号表示):
(l)W、Y、Z 三种元素的第一电离能由大到小的顺序为
(2)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键)
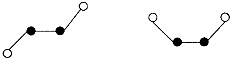
该分子中Y原子的杂化方式是
(3)W2-2阴离子的电子式为
(4)YQ3分子的空间构型为
(5)科学家通过X射线探明RZ的晶体结构与NaCl晶体结构相似.那么在RZ晶体中距离R2+最近且等距离的R2+有
(6)已知非整数比化合物R0.95Z,其晶体结构与NaCI相似,但由于R、Z离子个数比小于1:1,故晶体存在缺陷.R0.95Z可表示为
A、R
2+ 0.45 |
3+ 0.5 |
2+ 0.25 |
3+ 0.70 |
2+ 0.15 |
3+ 0.80 |
【化学--选修3物质结构与性质】
X、Y、Z、W、R为前四周期原予序数依次增大的五种元素,X、Y、Z、W为同一周期相邻元素,Z元素原子核外电子的运动状态共有8种;R元素与比它核电荷数大的另外两种元素位于第四周期同一族.
(l)X的一种核素用于鉴定文物年代,该核素的符号为 .
(2)X、Y、Z、W四种元素第一电离能由大到小的顺序为 (用元素符号表示).
(3)用氢键表示式写出W的气态氢化物水溶液中不同种分子间存在的氢键 .
(4)Y的一种氢化物分子中共有18个电子,该分子中存在的共价键类型有 (填选项字母).
A.非极性键 B.极性键C.S-SO- 键D.S-PO-键E.p-p键 F.s-sP3O-键 G.SP3-sP3O-键H.SP3-3P3π键
(5)R的基态原子的价层电子排布式为 ,R元素位于周期表的 区.
(6)R单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如图所示.图A中原子堆积方式为 ,A、B中实际含有的R原子个数之比 .A、B晶胞的棱长分别为a cm和b cm,则A、B两种晶体的密度之比为 .
查看习题详情和答案>>
X、Y、Z、W、R为前四周期原予序数依次增大的五种元素,X、Y、Z、W为同一周期相邻元素,Z元素原子核外电子的运动状态共有8种;R元素与比它核电荷数大的另外两种元素位于第四周期同一族.
(l)X的一种核素用于鉴定文物年代,该核素的符号为
(2)X、Y、Z、W四种元素第一电离能由大到小的顺序为
(3)用氢键表示式写出W的气态氢化物水溶液中不同种分子间存在的氢键
(4)Y的一种氢化物分子中共有18个电子,该分子中存在的共价键类型有
A.非极性键 B.极性键C.S-SO- 键D.S-PO-键E.p-p键 F.s-sP3O-键 G.SP3-sP3O-键H.SP3-3P3π键
(5)R的基态原子的价层电子排布式为

(6)R单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如图所示.图A中原子堆积方式为
(12分)有机物A(C11H12O2)可调配果味香精。可用含碳、氢、氧三种元素的有机物B和C为原料合成A。
(1)B的蒸汽密度是同温同压下氢气密度的23倍,分子中碳、氢原子个数比为1:3。有机物B的分子式为 。
(2)有机物C的分子式为C7H8O,C能与钠反应,不与氢氧化钠溶液反应,也不能使溴的四氯化碳溶液褪色。C的结构简式为 ,C与苯酚是否互为同系物: (填“是”或“否”)
(3)已知两个醛分子间能发生如下反应: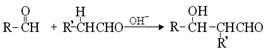 (﹣R、﹣R’表示氢原子或烃基)
(﹣R、﹣R’表示氢原子或烃基)
用B和C为原料按如下路线合成A: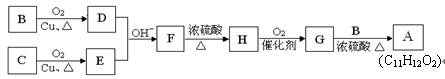
①上述合成过程中涉及到的反应类型有: (填写序号)
a取代反应;b 加成反应;c 消去反应;d 氧化反应;
②写出D与银氨溶液反应的化学方程式: 。
③ F的结构简式为: 。
④写出G和B反应生成A的化学方程式: 。
(4)F的同分异构体有多种,写出既能发生银镜反应又能发生水解反应,且苯环上只有一个取代基的所有同分异构体的结构简式 。