网址:http://m.1010jiajiao.com/timu3_id_332739[举报]
现拟从芳香烃
 出发来合成A,合成路线如下:
出发来合成A,合成路线如下: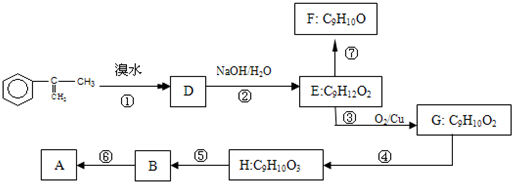
已知:烯醇结构不稳定,会自动异构化为醛:即R-CH=CH-OH→R-CH2-CHO.
(1)B中官能团的名称
(2)反应⑦属于消去反应
A加成反应 B消去反应 C氧化反应 D取代反应
(3)写出反应⑥的化学方程式:
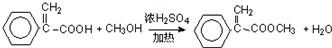

(4)反应⑦生成的有机物F有两种可能,结构简式分别为
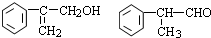
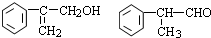
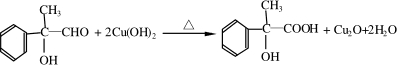
(5)①写出G与新制Cu(OH)2反应的方程式

②与G互为同分异构体,能与NaHCO3溶液反应,且苯环上的一卤代物只有两种的G同分异构体有
(6)A在一定条件下能生成一种高分子化合物,写出该反应的化学方程式:


| X | Y | |
| Z | W |
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为
(3)AW3可用于净水,其原理是
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提离反应速率,又能提高原料转化率的是
a.升高温度
b.加入催化剂
c.将X的简单气态氢化物及时移离
d.增大反应体系的压强
(5)标准状况下,2.24L X的简单气态氢化物被200mL 1mol?L-1 X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用WY2(沸点9.9℃)氧化除去CN-的离子方程式:
(14分)A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B与Z的最外层电子数之比为2︰3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1) X在周期表中的位置是_____________________________。
(2) 化合物Y2X2的电子式为 ;它含有的化学键类型有 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3) A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为_____________________________________。
(4) A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为_____________________________________。
(5) 写出化合物Y2X2与水反应的离子方程式____________________________。
(6) B的最高价氧化物的结构式为____________________________________。
查看习题详情和答案>>
(14分)A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B与Z的最外层电子数之比为2︰3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1) X在周期表中的位置是_____________________________。
(2) 化合物Y2X2的电子式为 ;它含有的化学键类型有 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3) A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为_____________________________________。
(4) A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为_____________________________________。
(5) 写出化合物Y2X2与水反应的离子方程式____________________________。
(6) B的最高价氧化物的结构式为____________________________________。
查看习题详情和答案>>
A、Y为常见金属单质,X为常见非金属单质。常温下X、G、H、I为气体,C为液体。B是由三种元素组成的盐,加热时发生分解生成两种气体,冷却后又可化合得到B。有关物质之间的转化关系如下图(部分反应条件及生成物略去)
请填写下列空白:
(1)B的电子式为 ;
(2)D固体可用于净水,请用相应的离子方程式及简单文字说明原因:
;
(3)反应⑥的化学方程式为 ;
反应④在冶金工业上属于 (填金属的冶炼方法);
(4)从D的结晶水合物制备D的无水晶体的操作为 ;
(5)反应②的化学方程式为 ;
反应③的离子方程式为 ;
(6)收集一试管H,将其倒置于水槽中,然后向试管中通入一定量的O2使试管内液面上升,最终剩余气体占试管容积的一半,则原有H与所通入O2的体积比为 。
查看习题详情和答案>>