网址:http://m.1010jiajiao.com/timu3_id_331998[举报]
(1)A、B、C的第一电离能由小到大的顺序为
(2)X是含有
(3)A的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为
(4)Y分子的空间构型为
(5)一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(6)Y是一种易液化的气体,请简述其易液化的原因
(7)写出E2+的电子排布式
A、B、C、D四种短周期元素的原子半径依次减小,D能分别与A、B、C形成电子总数相等的分子X、Y、Z.C原子的最外层电子排布为nsnnp2n.E的原子序数为29.
(1)A、B、C的第一电离能由小到大的顺序为________(用元素符号表示).
(2)X是含有________键(填“非极性”或“极性”,下同)的________分子.
(3)A的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为________.
(4)Y分子的空间构型为________,其中心原子采取________杂化.
(5)一种由B、C组成的化合物与AC2互为等电子体,其化学式为________.
(6)Y是一种易液化的气体,请简述其易液化的原因________________.
(7)写出E2+的电子排布式________,并写出E2+在Z中通入足量Y得到深蓝色溶液的离子方程式________.
元素 | 符号 | 名称 | 四种元素单质间的反应 |
A |
|
|
|
B |
|
| |
C |
|
| |
D |
|
|
已知:B原子有3个能级且各能级电子数相等;D原子最外能层P能级上有2个未成对电子,E是同周期元素中第一电离能最小的元素;F是同周期元素中原子半径最小的元素;A是非金属元素,且A、C、F可形成离子化合物.
请回答:
(1)A、D形成的三原子分子中心原子杂化类型是
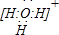
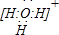
(2)元素A、D、F形成的原子数之比为1:1:1的化合物的电子式为


(3)请用电子式表示D、E原子个数比为1:1的化合物的形成过程


(4)在B原子与A形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写出其中一种分子的名称
Ⅱ.某合金由 X、Y、Z三种元素组成,这三种元素位于周期表中前四周期,X是主要成分元素,X的基态原子中有4个未成对电子.Y的含量不低于11%,否则不能生成致密氧化膜YO3防止腐蚀,Y与X同周期,且原子核外未成对电子数最多.Z位于周期表中第4行、第10列.
(5)请写出X、Y、Z的元素符号及原子序数X
(6)请写出Z的原子核外电子排布式
(14分)Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+ 的核外电子排布式是 。
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的 形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲>乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4) Q、R、X、Y四种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)
(5)R的氢化物的熔沸点比同主族其它元素氢化物的熔沸点高,原因是R氢化物________
________________________________________________________________________。
(6)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
(7)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 。
查看习题详情和答案>>