ժҪ��23��ͨ�����ǰѲ�1mol ij��ѧ�������յ��������ɸû�ѧ���ļ���.���ܵĴ�С���Ժ�����ѧ����ǿ��.Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H).��ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ�. ��ѧ�� P-H Si-Cl H-H P-P Si-Si Si-C ����/ KJ��mol-1 326 360 436 197 176 347 ��ش���������: �� �Ƚ������������ʵ��۵�ߵ� SiC Si, Si ,PH3 HF, PCl5 SiCl4 (2) PH3�ڼ��������·ֽ����ɰ�������.4 PH3(g) === 6H2(g)+P4(s), �÷�Ӧ�ķ�Ӧ�ȡ�H = KJ/mol (3)Һ̬�л���2.3g��һ������������ϵ�ȼ.ǡ����ȫȼ��.����2.7gH2O��2.24LCO2���ų�68.35kJ������.��÷�Ӧ���Ȼ�ѧ����ʽΪ: (4)��Ӧ��Ҳ������ʵ�鷽���ⶨ.����n mL0.50mol/L��������n mL1.10mol/L��NaOH ��Һ���.�������Һ�ܶȾ�����Ϊ1g/mL.��Һ�ı�����Ϊ4.18J/ ��Ӧǰ�����¶�Ϊt1.����������Һ�¶�Ϊt2.��Ӧ������Һ�¶�Ϊt3.��ˮ���к� �ȵļ������ʽΪ��H=
��ַ��http://m.1010jiajiao.com/timu3_id_330299[�ٱ�]
ͨ�����ǰѲ�1mol ij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ���ʱ䣨��H������ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
|
ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ķ�Ӧ�ȵ��ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
��ش��������⣺
��1����֪Si��SiC��SiO2�ۻ�ʱ�������������ѧ�����Ƚ������������ʵ��۵�ߵͣ��������������SiC
��2����ҵ�ϸߴ����ͨ�����з�Ӧ��ȡ��
SiCl4��g��+2H2��g��
Si��s��+4HCl��g����
��2mol H2���ɸߴ�����
�鿴ϰ������ʹ�>>
| ��ѧ�� | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| ����/ kJ?mol-1 |
460 | 360 | 436 | 431 | 176 | 347 |
��1����֪Si��SiC��SiO2�ۻ�ʱ�������������ѧ�����Ƚ������������ʵ��۵�ߵͣ��������������SiC
��
��
Si��Si��
��
SiO2��2����ҵ�ϸߴ����ͨ�����з�Ӧ��ȡ��
SiCl4��g��+2H2��g��
| ||
��2mol H2���ɸߴ�����
����
����
������ա��ų���������236
236
kJ�� ͨ�����ǰѲ�1mol ij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H����
ͨ�����ǰѲ�1mol ij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H����| ��ѧ�� | Cl-Cl | H-H | H-Cl | N��N |
| ����/kJ?mol | 243 | 436 | 431 | 946 |
a 2HCl��g��=H2��g��+Cl2��g������H=
+183kJ/mol
+183kJ/mol
b N2��g��+3H2��g��=2NH3��g����H=-92kJ/mol����N-H���ļ�����
391
391
kJ?mol��2��1mol NO2��1mol CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ
NO2��g��+CO��g��=CO2��g��+NO��g��
NO2��g��+CO��g��=CO2��g��+NO��g��
��H=-234kJ?mol-1
��H=-234kJ?mol-1
��3����֪�ڳ��³�ѹ�£�
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H1
��2CO ��g��+O2��g��=2CO2��g����H2
��H2O��g��=H2O��l����H3
��CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
��4����֪��2Al ��s��+
| 3 |
| 2 |
2Fe ��s��+
| 3 |
| 2 |
��д����������������ĩ�������ȷ�Ӧ���Ȼ�ѧ����ʽ
2Al��s��+Fe2O3��s���TAl2O3��s��+2Fe��s����H=-828.42kJmol-1
2Al��s��+Fe2O3��s���TAl2O3��s��+2Fe��s����H=-828.42kJmol-1
�� ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ���Թ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ���Թ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ| ��ѧ�� | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| ����/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
��1���Ƚ������������ʵ��۵�ߵͣ������������SiC
��2����ͼ���������ĵġ���ʾ�辧���е�һ��ԭ�ӣ�����������Ķ����á���ʾ����֮���ڵĹ�ԭ�ӣ�
��3����ҵ���øߴ����ͨ�����з�Ӧ��ȡ��SiCl4��g��+2H2��g��
| ||
21.ͨ�����ǰѲ�1mol ij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
��ѧ�� | Si��O | Si��Cl | H��H | H��Cl | Si��Si | Si��C |
����/ kJ��mol��1 | 460 | 360 | 436 | 431 | 176 | 347 |
��ش��������⣺
�� �Ƚ������������ʵ��۵�ߵͣ����
SiC______ Si�� SiCl4 ______ SiO2
�� ͼ���������ĵġ���ʾ�辧���е�һ��ԭ�ӣ�
����������Ķ����á���ʾ����֮���ڵĹ�ԭ�ӡ�
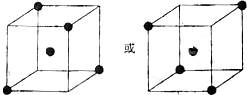
�� ��ҵ�ϸߴ����ͨ�����з�Ӧ��ȡ��
SiCl4 (g) + 2H2(g) ![]() Si(s) + 4HCl(g)
Si(s) + 4HCl(g)
�÷�Ӧ�ķ�Ӧ�ȡ�H = ___________ KJ/mol