网址:http://m.1010jiajiao.com/timu3_id_329700[举报]
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是 (填具体离子符号);由A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于 。
(2)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为: 。
(3)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式为 ,
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LA2时, NaCl溶液的PH= (假设电解过程中溶液的体积不变) 。
(4)可逆反应2EC2(气)+C2(气) 2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2 和2molEC2,使V (A ) = V (
B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t
( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2 的转化率:a( A ) _a( B )。
2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2 和2molEC2,使V (A ) = V (
B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t
( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2 的转化率:a( A ) _a( B )。

(5)欲比较C和E两元素的非金属性相对强弱,可采取的措施有 (填“序号”)。
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易
查看习题详情和答案>>
A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,其余均为常见化合物,J是一种黑色固体,I的浓溶液具有还原性,从A-I的所有物质之间有如下的转化关系:
回答下列问题:
(1)写出物质C的构成元素在周期表中的位置______.
(2)写出B与F反应的化学方程式______.
(3)由E的饱和溶液可以制得胶体,具体制备方法是:______,用化学方程式表示该过程的原理:______.若要提纯该胶体,采用的操作方法叫______.此液体具有的性质是______(填写序号字母)
a.光束通过该液体时形成光亮的“通路”?
b.向液体中逐滴加入足量氢碘酸,先有沉淀产生,后沉淀逐渐溶解,再滴入几滴淀粉溶液,溶液变为蓝色
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧,得红棕色固体?
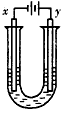
另取少量上述胶体置于U型管中,按如图装置图连接好装置.通电一小段时间后,X极附近的现象是______.
(4)取少量上述胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液颜色逐渐变浅,最终得到黄色的溶液,发生此变化的离子方程式为______.
(5)G的水溶液显______性(填酸或碱);原因是(用离子方程式表 示)______.
(6)J在H2O2分解反应中作催化剂.若将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是______.
查看习题详情和答案>>
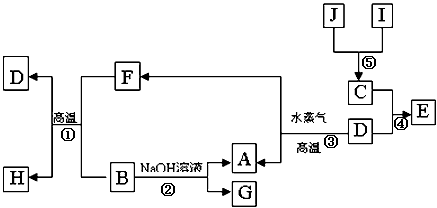
(1)写出物质C的构成元素在周期表中的位置___________________;
(2)写出B与F反应的化学方程式______________________________。
(3)由E的饱和溶液可以制得胶体,具体制备方法是:______________________。用化学方程式表示该过程的原理:______________________________。若要提纯该胶体,采用的操作方法叫___________。此液体具有的性质是___________(填写序号字母)
a.光束通过该液体时形成光亮的“通路”
b.向液体中逐滴加入足量氢碘酸,先有沉淀产生,后沉淀逐渐溶解,再滴入几滴淀粉溶液,溶液变为蓝色
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧,得红棕色固体?
另取少量上述胶体置于U型管中,按下图装置图连接好装置。通电一小段时间后,X极附近的现象是______________________
(5)G的水溶液显________性(填酸或碱);原因是(用离子方程式表示)______________________。
(6)J在H2O2分解反应中作催化剂。若将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是____________________________。
(7)上述①--⑤5个化学反应中属于置换反应的有_________________(填序号)
(1)写出元素B的元素符号_________,元素B的氢化物的空间构型为__________。
(2)写出D原子形成简单离子的电子排布式________________。
(3)四种元素离子半径的大小顺序为__________,第一电离能最小的是__________。
(4)C的双原子单质分子中含有____个σ键和______个π键,元素C的三原子氢化物中,中心原子C的杂化方式为____________。
(5)元素A和C形成的化合物熔点高,硬度大,工业上常采用电解熔融该化合物的方法来制备单质A。由此 可推断A、C形成的化合物为__________晶体。
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是 (填具体离子符号);由A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于 。
(2)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为: 。
(3)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式为 ,
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LA2时, NaCl溶液的PH= (假设电解过程中溶液的体积不变) 。
(4)可逆反应2EC2(气)+C2(气)
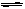 2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =" V" ( B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t ( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2的转化率:a( A ) _a( B )。
2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =" V" ( B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t ( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2的转化率:a( A ) _a( B )。 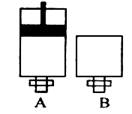
(5)欲比较C和E两元素的非金属性相对强弱,可采取的措施有 (填“序号”)。
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易