网址:http://m.1010jiajiao.com/timu3_id_329543[举报]
(15分) 已知某有机物A的质谱图显示其相对分子质量为84,则
(1) 烃A的分子式为_____________。
(2) 若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为__________________。
(3) 若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式为 。
(4) 比烃A少一个碳原子且能使溴水褪色的A的同系物有________种同分异构体。
(5)若烃A红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
反应②的化学方程式为 ______________________ ;C的化学名称为 ___________ ;
E2的结构简式是 ________________ ;⑥的反应类型是 _____________ 。
查看习题详情和答案>>
﹙15分﹚已知

A与芳香族化合物B在一定条件下反生成C,进一步反应生成抗氧化剂阿魏酸(见下图)

A的相对分子质量是104,1molA与足量NaHCO3溶液反应生成2mol气体。
(1)A的结构简式是________________。
(2)在中学学过知识里 B不可能发生的反应是________ (填序号)
a、取代反应 b、加成反应c、氧化反应d、 还原反应e、水解反应 f、显色反应
(3)等物质的量C分别与足量的Na、浓溴水、NaOH、NaHCO3反应时消耗Na、Br2、NaOH、NaHCO3的物质的量之比是
(4)写出C与足量的Na2CO3的化学方程式为:
(5)写出符合下列条件的阿魏酸的一种同分异构体的结构简式: 。
①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种;
③1mol该同分异构体与足量NaHCO3反应生成2mol CO2气体;
(6)写出利用阿魏酸在一定条件下生成抗氧化性的高分子化合物的方程式:
___________________________________________________________________。
查看习题详情和答案>>
(15分)已知CaSO4受热分解,由于受热温度不同,气体成分也不同。气体成分可能为SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组准备通过系列实验探究CaSO4分解生成的气体,进而确定CaSO4分解的化学方程式。
【提出猜想】
Ⅰ.所得气体的成分可能只含 SO3一种;
Ⅱ.所得气体的成分可能含有 二种;(填分子式)
Ⅲ.所得气体的成分可能含有 SO2、SO3、O2三种。
【设计实验】
该化学课外活动小组准备通过测定D装置的增重以及量筒中水的体积,来探究CaSO4分解生成的气体成分,进而确定CaSO4分解的化学方程式。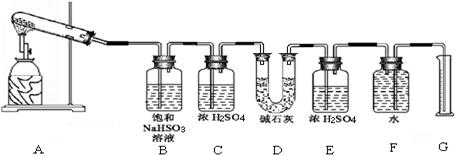
【实验过程】
根据上述实验方案进行试验。已知实验结束时,CaSO4完全分解。
请结合以下实验现象和记录的实验数据进行分析:
(1)若实验结束时,G中量筒没有收集到水,则证明猜想 正确。(填Ⅰ或Ⅱ或Ⅲ)
(2)若实验结束时,装置D的总质量增加,能否断定气体产物中一定含有SO2而不含SO3?请说明理由: 。
(3)该实验设计中,容易给测 定带来较大误差的因素有 。
定带来较大误差的因素有 。
(写出一种即可)
(4)经改进后,有两组同学进行该实验,由于加热时的温度不同,实验测得数据也不同,
相关数据如下:
| 实验小组 | 称取CaSO4 的质量(g) | 装置D增加 的质量(g) | 量取气体体积的装置测量的气体体积 (折算成标准状况下气体的体积) (mL) |
| 一 | 4.08 | 2. 56 56 | 224 |
| 二 | 5.44 | 2.56 | 448 |
第二组: 。 查看习题详情和答案>>
(本小题15分)已知一定条件下丙烯的浓HBr能发生如下反应:
CH3-CH=CH2 + H-Br CH3--CH3
化合物A和A’互为同分异构体,元素分析含溴58.4%(其它元素数据不全,下同)。A和A’有如下系列反应,其中气态物质B是烃,含碳85.7%;C’不发生类似图中C的系列转化;E为酸性物质,其中碳氢含量共为63.6%。
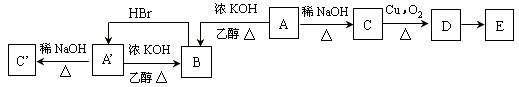
请回答下列问题:
(1)写出结构简式:A ,B: 。
(2)写出下列转化关系的化学方程式:
①B→A’ : 。
②C→D: 。
③D→E: 。
(3)简述检验A中含有溴元素的实验方法:
。
查看习题详情和答案>>(15分) 已知①~④均为工业生产及应用的常见反应。其中常温下B、D、J、P气体,E为分子中原子个数比为1∶l的液体。A的相对分子质量为120。(个别反应的产物已略去)
试回答下列问题:
(1)反应F与N溶液反应的离子方程式为________________________________________;
(2)反应⑤中当有1mol电子转移时,氧化剂消耗 g。
(3)反应④的离子方程式为______________________________;
右图是该反应原理的示意图,该装置中使用的是 (填“阴”或“阳”)离子交换膜。图中从d处收集到的是 。
(4)工业上由D制取I的过程可表示为:
由D与B反应生成X的反应所用的设备是
①高炉 ②沸腾炉 ③接触室 ④分馏塔 ⑤吸收塔
已知400℃ 101Kpa时,2D(g) + B(g)![]() 2X(g);△H = – 196.6KJ/mol,当2 mol D与1mol B在该条件下反应达平衡时反应放热186.8 KJ。
2X(g);△H = – 196.6KJ/mol,当2 mol D与1mol B在该条件下反应达平衡时反应放热186.8 KJ。
在实际生产中综合考虑各种因素,为提高D的转化率,工业选择了以下哪些条件______
①适当升高温度 ②增大压强 ③使用合适的催化剂 ④及时移走生成物 ⑤适当增大B的浓度 ⑥将反应物与生成物在热交换器中进行热交换
查看习题详情和答案>>