摘要:9.A和B是第二或第三周期元素.可在同一周期.也可以在不同周期.两者可形成AmBn型离子化合物.若A的原子序数为x.则B的原子序数不可能是 A.x-m-n+16 B.x+m+n-8 C.x-m-n+8 D.x-m-n
网址:http://m.1010jiajiao.com/timu3_id_329479[举报]
| |||||||||||||||||||||||||||||||||
A、B、C是中学化学中常见的三种短周期元素.已知:①A元素原子最外层电子数是次外层电子数的2倍;②B元素最高正价与最低负价的代数和为2;③C元素有多种化合价,且常温下C元素的单质与某种一元强碱溶液反应,可得到两种含C元素的化合物;④B、C两种元素质子数之和是A元素质子数的4倍.
(1)写出A元素在周期表中的位置
(2)写出C的单质和强碱溶液反应的离子方程式
(3)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的B4气态分子.B4分子结构与白磷分子结构相似 ,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:
,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:
(4)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构.X遇水蒸气可形成一种常见的漂白性物质.则X的结构式为
 ,X与水反应的化学方程式是
,X与水反应的化学方程式是
(5)A、B两种元素可形成一种硬度比金刚石还大的化合物Y.在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构.则Y的化学式为
(6)B2H4是一种可燃性液体,其水溶液呈弱碱性,是因为溶液中存在平衡:H2B-BH2+H2O?
查看习题详情和答案>>
(1)写出A元素在周期表中的位置
第二周期ⅣA族
第二周期ⅣA族
;(2)写出C的单质和强碱溶液反应的离子方程式
C12+2OH-=ClO-+Cl-+H2O
C12+2OH-=ClO-+Cl-+H2O
;(3)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的B4气态分子.B4分子结构与白磷分子结构相似
 ,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:
,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:N4(g)═2N2(g)△H=-882kJ/mol
N4(g)═2N2(g)△H=-882kJ/mol
;(4)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构.X遇水蒸气可形成一种常见的漂白性物质.则X的结构式为


NCl3+3H2O═NH3+3HClO
NCl3+3H2O═NH3+3HClO
;(5)A、B两种元素可形成一种硬度比金刚石还大的化合物Y.在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构.则Y的化学式为
C3N4
C3N4
,Y晶体的熔点比金刚石熔点高
高
(填“高”或“低”);(6)B2H4是一种可燃性液体,其水溶液呈弱碱性,是因为溶液中存在平衡:H2B-BH2+H2O?
H2N-NH3++OH-(或N2H5++OH-)
H2N-NH3++OH-(或N2H5++OH-)
.都由短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱.E在足量空气中燃烧产生刺激性气味气体G,G在大气中能导致酸雨的形成.E被足量氢氧化钠溶液吸收得到无色溶液F,溶液F在空气中长期放置发生反应,生成物之一为H. H与一种相对分子质量为78的供氧剂的结构和化学性质相似,其溶液显黄色.
请回答下列问题:
(1)组成单质A的元素位于周期表中的位置
(2)指出H物质中的化学键类型
(3)写出B与氢氧化钠溶液反应的离子方程式:
(4)E被足量NaOH溶液吸收得到溶液中的离子浓度由大到小关系是
(5)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.当生成2mol二氧化氯时,转移电子
(6)溶液F在空气中长期放置生成H的化学反应方程式为:
查看习题详情和答案>>
请回答下列问题:
(1)组成单质A的元素位于周期表中的位置
第三周期ⅥA
第三周期ⅥA
.(2)指出H物质中的化学键类型
离子键、共价健
离子键、共价健
.(3)写出B与氢氧化钠溶液反应的离子方程式:
2Al+2OH-+2H2O═2AlO-2+3H2↑
2Al+2OH-+2H2O═2AlO-2+3H2↑
.(4)E被足量NaOH溶液吸收得到溶液中的离子浓度由大到小关系是
C(Na+)>C(S2-)>C(OH-)>C(HS-)>C(H+)
C(Na+)>C(S2-)>C(OH-)>C(HS-)>C(H+)
.(5)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.当生成2mol二氧化氯时,转移电子
2
2
mol.(6)溶液F在空气中长期放置生成H的化学反应方程式为:
4Na2S+O2+2H2O═4NaOH+2Na2S2(或2Na2S+O2+2H2O═4NaOH+2S,Na2S+S═Na2S2)
4Na2S+O2+2H2O═4NaOH+2Na2S2(或2Na2S+O2+2H2O═4NaOH+2S,Na2S+S═Na2S2)
.四种短周期元素A、B、C、D的性质或结构信息如下.
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置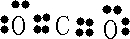
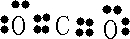 .
.
②A元素的单质与物质甲发生反应的离子方程式
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
查看习题详情和答案>>
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置
第二周期ⅥA族
第二周期ⅥA族
,请写出BC2分子的电子式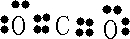
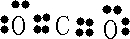
②A元素的单质与物质甲发生反应的离子方程式
Cl2+H2O H++Cl-+HClO
H++Cl-+HClO
 H++Cl-+HClO
H++Cl-+HClOCl2+H2O H++Cl-+HClO
H++Cl-+HClO
. H++Cl-+HClO
H++Cl-+HClO③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
CH4-8e-+10OH-=CO32-+7H2O
CH4-8e-+10OH-=CO32-+7H2O
;正极2O2+8e-+4H2O=8OH-
2O2+8e-+4H2O=8OH-
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
2Cl-2e-=Cl2↑
2Cl-2e-=Cl2↑
.检验Y电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
.②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
13
13
(假设电解液的体积保持不变,常温下)
