摘要: 将m克CaCO3与n克KHCO3分别加入100毫升0.5摩/升盐酸中.若反应后两种溶液的质 量相等.则m与n的关系是 (A) m=n.且均≤2.5 (B) m=n,且均>2.5 (C) m=n.且均≥5 (D) m<n<2.5
网址:http://m.1010jiajiao.com/timu3_id_329245[举报]
将m g CaCO3与n g KHCO3分别加入100mL 0将m g CaCO3与n g KHCO3分别加入100mL 0.5mol/L盐酸中,若反应后两种溶液的质量相等,则m与n的关系是
- A.m=n≤2.5
- B.m=n>2.5
- C.m=n≥5
- D.m<n<2.5
将m g CaCO3与n g KHCO3分别加入100mL0.5mol/L盐酸中,若反应后两种溶液的质量相等,则m与n的关系是
[ ]
A. m=n, 且均≤2.5 B. m=n, 且均>2.5
C. m=n, 且均≥5 D. m<n<2.5
查看习题详情和答案>>将m g CaCO3与n g KHCO3分别加入100mL 0.5mol/L的盐酸中.若反应后两种溶液的质量相等,则m与n的关系是
[ ]
A.m=n≤2.5
B.m=n>2.5
C.m=n≥5
D.m<n<2.5
将m g CaCO3与n g KHCO3分别加入100mL 0.5mol/L的盐酸中.若反应后两种溶液的质量相等,则m与n的关系是
[ ]
A.m=n≤2.5
B.m=n>2.5
C.m=n≥5
D.m<n<2.5
如图1是元素周期表的一部分.
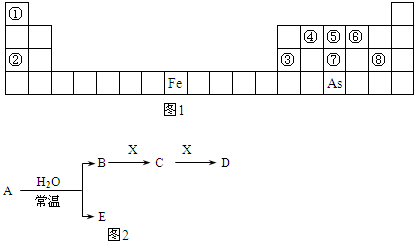
Ⅰ.用化学用语回答下列问题:
(1)②、⑥、⑧的离子半径由大到小的顺序为
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)As的原子结构示意图为
 ;其氢化物的化学式为
;其氢化物的化学式为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂.As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
Ⅱ.A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物.已知A、B、C、D、E、X存在如图2所示转化关系(部分生成物和反应条件略去).
若常温下A为红棕色气体,B为强酸,X为常见金属单质
(5)A与水反应的化学方程式为
(6)工业上常用热还原法冶炼X,写出其化学方程式
(7)某温度下(>100℃)若m克X与H2O反应放出QKJ (Q>O)的热量.写出该反应的热化学方程式
(8)少量X与B的稀溶液反应生成C的离子反应方程式为
查看习题详情和答案>>

Ⅰ.用化学用语回答下列问题:
(1)②、⑥、⑧的离子半径由大到小的顺序为
Clˉ>O2ˉ>Na+
Clˉ>O2ˉ>Na+
.(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
HClO4>H3PO4>H2CO3
HClO4>H3PO4>H2CO3
.(3)As的原子结构示意图为


AsH3
AsH3
.(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂.As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
5NaClO+2As+3H2O═2H3AsO4+5NaCl
5NaClO+2As+3H2O═2H3AsO4+5NaCl
,当消耗1mol还原剂时,电子转移了5
5
mol.Ⅱ.A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物.已知A、B、C、D、E、X存在如图2所示转化关系(部分生成物和反应条件略去).
若常温下A为红棕色气体,B为强酸,X为常见金属单质
(5)A与水反应的化学方程式为
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.(6)工业上常用热还原法冶炼X,写出其化学方程式
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(7)某温度下(>100℃)若m克X与H2O反应放出QKJ (Q>O)的热量.写出该反应的热化学方程式
3Fe(s)+4H2O(g)═Fe3O4(s)+4H2(g)△H=-
kJ/mol
| 168Q |
| m |
3Fe(s)+4H2O(g)═Fe3O4(s)+4H2(g)△H=-
kJ/mol
.| 168Q |
| m |
(8)少量X与B的稀溶液反应生成C的离子反应方程式为
Fe+4H++NO3ˉ=Fe3++NO↑+2H2O
Fe+4H++NO3ˉ=Fe3++NO↑+2H2O
.