摘要:9.X.Y.W为常见的四种单质.常温下X是固体.Y是液体.Z是无色气体.W为黄绿色气体.其反应关系如下.其中B的溶液显强酸性.
网址:http://m.1010jiajiao.com/timu3_id_328910[举报]
X、Y、W、Z为常见的四种单质,X是日常生活中用途最为广泛的金属,常温下Y是液体,Z是无色气体,W为黄绿色气体。其反应关系如下,其中B的溶液呈强酸性。

(1)W在元素周期表中的位置是 。
(2)根据反应推断Y、D的化学式:Y ,D 。
(3)检验A溶液中阳离子的方法 。
(4)写出C与少量W反应的化学方程式: 。
查看习题详情和答案>>X、Y、Z、W四种元素的原子序数依次增大,且均为短周期元素.X原子最外层电子数是次外层电子数的2倍;Y有两种常见的同素异形体,其中一种是很好的脱色剂和消毒剂.Z、W原子最外层电子数之和是X原子最外层电子数的2倍,且Y与W同族.请填空:
(1)固态的XY2属于
(2)W与X可形成化合物XW2.①XW2为
(3)工业制Z的方法为
(4)WY2→WY3的工业反应条件是
查看习题详情和答案>>
(1)固态的XY2属于
分子
分子
晶体.X的氢化物中含氢的质量分数最高的分子的空间构型为正四面体
正四面体
.(2)W与X可形成化合物XW2.①XW2为
非极性
非极性
(填“极性”或“非极性”)分子;②Z的单质在XY2气体中燃烧的现象为镁条在二氧化碳中剧烈燃烧,生成白色粉末,在瓶的内壁有黑色固体附着
镁条在二氧化碳中剧烈燃烧,生成白色粉末,在瓶的内壁有黑色固体附着
.(3)工业制Z的方法为
电解法
电解法
.(4)WY2→WY3的工业反应条件是
高温常压催化剂
高温常压催化剂
其方程式为2SO2+O2
2SO3
| 催化剂 |
| △ |
2SO2+O2
2SO3
.| 催化剂 |
| △ |
X、Y、Z、W为四种短周期元素.X元素的原子最外层电子数是核外电子层数的3倍;Y元素的最高正价与最低负价的代数和为6;Z在地球中的含量仅次于氧;Y、Z、W同周期,W的常见化合价为+2价.下列说法不正确的是( )
查看习题详情和答案>>
X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大.X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少、构成蛋白质的重要组成元素;Z的基态原子核外9个轨道上填充了电子,且核外有2个未成对电子,与Y不同族;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体.
(1)常温常压下Z单质是 晶体(填类型),微粒间通过 形成晶体(填微粒间相互作用的类型).Y2分子中存在σ键和π键个数之比为 .
(2)X-H和Y-H属于极性共价键,其中极性较强的键是 (X、Y用元素符号表示).X的第一电离能比Y的 (填“大”或“小“).
(3)写出X单质与Z的最高价氧化物对应的水化物的浓溶液反应的化学方程式
(4)W的基态原子的外围电子排布式是 .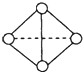
(5)已知一种分子Y4分子结构如图所示:断裂1molY-Y吸收167kJ的热量,生成1molY≡Y放出942kJ热量.试写出由Y4气态分子变成Y2气态分子的热化学方程式 .
查看习题详情和答案>>
(1)常温常压下Z单质是
(2)X-H和Y-H属于极性共价键,其中极性较强的键是
(3)写出X单质与Z的最高价氧化物对应的水化物的浓溶液反应的化学方程式
(4)W的基态原子的外围电子排布式是

(5)已知一种分子Y4分子结构如图所示:断裂1molY-Y吸收167kJ的热量,生成1molY≡Y放出942kJ热量.试写出由Y4气态分子变成Y2气态分子的热化学方程式
X、Y、Z、W、H是元素周期表前四周期中的五种常见元素,其相关信息如下表:
回答下列问题(用化学用语作答)
(1)下列选项中能作为判断Y和Z 的非金属性强弱的依据有(填字母编号)
a.Y和Z的单质的熔点高低
b.Y和Z的氢化物的稳定性强弱
c.Y和Z的氢化物的沸点高低
d.Y和Z的最高价氧化物对应的水化物的酸性强弱
(2)用电子式表示X的最简单氢化物的形成过程 ;
(3)Y元素在元素周期表中的位置为 .化合物A由Y、Z、W三种元素组成,其水溶液能够溶解W的单质.化合物A的溶液能够净水,原因是 (用离子方程式解释);
(4)取100mL1mol/L(3)中 A的溶液,加入W单质和H单质的混合物粉末共6g充分搅拌后,固体完全溶解,往反应后溶液中加入KSCN溶液,无明显现象.则混合物粉末中W单质的质量分数为 ;
(5)取100mL物质的量浓度均为1mol/L的X的最高价含氧酸和Y的最高价含氧酸的混合稀溶液,加入足量H单质的粉末充分搅拌,最多能溶解该粉末 g.
查看习题详情和答案>>
| 元素 | 相关信息 |
| X | X元素在空气中含量最高 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同主族,原子半径:Y>Z |
| W | W元素的一种氧化物具有磁性 |
| H | H元素形成的盐溶液一般呈蓝色 |
(1)下列选项中能作为判断Y和Z 的非金属性强弱的依据有(填字母编号)
a.Y和Z的单质的熔点高低
b.Y和Z的氢化物的稳定性强弱
c.Y和Z的氢化物的沸点高低
d.Y和Z的最高价氧化物对应的水化物的酸性强弱
(2)用电子式表示X的最简单氢化物的形成过程
(3)Y元素在元素周期表中的位置为
(4)取100mL1mol/L(3)中 A的溶液,加入W单质和H单质的混合物粉末共6g充分搅拌后,固体完全溶解,往反应后溶液中加入KSCN溶液,无明显现象.则混合物粉末中W单质的质量分数为
(5)取100mL物质的量浓度均为1mol/L的X的最高价含氧酸和Y的最高价含氧酸的混合稀溶液,加入足量H单质的粉末充分搅拌,最多能溶解该粉末