摘要: 0.04摩KMnO4固体.加热一段时间后.收集到a摩气体.在反应后的留固体中加入足量的浓盐酸.又收集到b摩气体.设此时Mn元素全部以Mn2+存在于溶液中.则: (1)a+b的取值范围为[答:0.08≤a+b<0.1] (2)计算若a+b=0.09摩时.残留固体的质量为多少克?[答:6克] [提示]:2KMnO4 =K2MnO4+MnO2+O2 2a摩 a摩 a摩 a摩 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O 0.04-2a K2MnO4+8HCl=2KCl+2MnCl2+2Cl2+4H2O a 2a MnO2+4HCl=MnCl2+Cl2+2H2O a a 可知:b=2a+a+= 因为a+b=a+=0.09.解得a=0.01摩 则O2质量为0.01×32=0.32克.残留固体质量为0.04×158-0.32=6克.
网址:http://m.1010jiajiao.com/timu3_id_328720[举报]
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是AgNO3溶液,电解之前在两极各滴入几滴石蕊试液,则
①Y电极上的电极反应式是
4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
,在Y极附近观察到的现象是
放出无色无味的气体,且溶液变红
放出无色无味的气体,且溶液变红
.②电解总反应离子方程式为
4Ag++2H2O═4Ag+O2↑+4H+
4Ag++2H2O═4Ag+O2↑+4H+
.(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是
纯铜
纯铜
,②Y电极的电极反应式是Cu-2e-=Cu2+
Cu-2e-=Cu2+
(说明:杂质发生的电极反应不必写出)
③假若电路中有0.04摩尔电子通过时,阴极增重
1.28
1.28
克.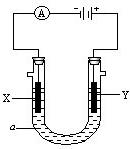 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解 液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解 液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: