摘要:0.1摩元素X的单质与氧气完全反应生成氧化物后.质量增加了4克.该氧化物的组成是----------------------------------------------------------------(C) A.XO B.X2O3 C.X2O5 D.XO3 [提示]:由题意可推知1摩尔X可增加40克.也就是摩氧元素.该氧化物的分子式初定为XO.再得出它的分子式为X2O5.
网址:http://m.1010jiajiao.com/timu3_id_328660[举报]
Ⅰ.根据下列数据判断元素X的相对原子质量.
(1)1.01×105 Pa,273℃时气态单质Xn的密度为d g/L,则X的相对原子质量为 .
(2)相同状况下,一定体积的气态氢化物HmX的质量是等体积NH3的2倍.则X的相对原子质量为 .
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为 .
Ⅱ.(1)20g A物质和14g B物质完全反应,生成8.8g C物质、3.6g D物质和0.2mol E物质,则E物质的摩尔质量为 .
(2)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为 ,其相对分子质量为 ,
X的相对原子质量为 ,该物质的化学式为 .
查看习题详情和答案>>
(1)1.01×105 Pa,273℃时气态单质Xn的密度为d g/L,则X的相对原子质量为
(2)相同状况下,一定体积的气态氢化物HmX的质量是等体积NH3的2倍.则X的相对原子质量为
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为
Ⅱ.(1)20g A物质和14g B物质完全反应,生成8.8g C物质、3.6g D物质和0.2mol E物质,则E物质的摩尔质量为
(2)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为
X的相对原子质量为
 (2011?百色模拟)有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据如图转化关系(反应条件及部分产物已略去),回答下列问题:
(2011?百色模拟)有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据如图转化关系(反应条件及部分产物已略去),回答下列问题:(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则
①A分子的空间构型为
三角锥形
三角锥形
.②反应I的化学方程式为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式
3NaN3=Na3N+4N2↑
3NaN3=Na3N+4N2↑
.(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120g?mol-1,则:
①将反应IV所得的溶液加热蒸干得到的晶体属于
离子
离子
晶体(填“离子”、“分子”、“原子”)②反应I的化学方程式为
4FeS2+11O2
2Fe2O3+8SO3
| ||
4FeS2+11O2
2Fe2O3+8SO3
.
| ||
③0.1mol的B(气态)全部转化为C(气态)时放出9.83kJ热量,请写出反应的热化学方程式
2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ/mol
2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ/mol
. 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后作答:
下表中列出五种短周期元素A、B、C、D、E的信息,请推断后作答:| 元素 | 有关信息 |
| A | 元素主要化合价为-2,原子半径为0.074n m |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102n m,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物的水化物,能按1:1电离出电子数相等的阴、阳离子 |
| E | 原子半径为0.075n m,最高价氧化物的水化物与其氢化物组成一种盐X |




(2)盐X水溶液显
酸
酸
(填“酸”“碱”“中”)性,用离子方程式解释其原因NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
. NH3?H2O+H+
NH3?H2O+H+(3)D2CA3的溶液与B的单质能发生反应,其反应的离子方程式为
SO32-+Cl2+H2O=SO42-+2H++2Cl-
SO32-+Cl2+H2O=SO42-+2H++2Cl-
.(4)已知E元素的某种氢化物Y与A2的摩尔质量相同.Y与空气组成的燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液.该燃料电池放电时,正极的电极反应式是
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.(5)如图是一个电解过程示意图.假设使用Y-空气燃料电池作为本过程的电源,铜片质量变化128g,则Y一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)
112
112
L.甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族.X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、F的焰色反应为黄色.在一定条件下,各物质相互转化关系如图.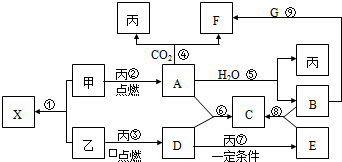
请回答:
(1)写化学式:丙
(2)X的电子式为
 ,G的空间构型是
,G的空间构型是
(3)写出反应⑤的化学反应方程式:
(4)写出B溶液与G反应生成F的离子方程式:
(5)在上图①-⑨的反应中,不属于氧化还原反应的是(填序号)
(6)将8g 乙在足量丙中燃烧,所得气体D通入100mL 3.5mol?L-1的B溶液中,完全吸收后,溶液中的溶质及其物质的量分别为
查看习题详情和答案>>

请回答:
(1)写化学式:丙
O2
O2
ESO3
SO3
(2)X的电子式为


直线型
直线型
.(3)写出反应⑤的化学反应方程式:
2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2H2O═4NaOH+O2↑
.(4)写出B溶液与G反应生成F的离子方程式:
CO2+2OH-═CO32-+H2O
CO2+2OH-═CO32-+H2O
.(5)在上图①-⑨的反应中,不属于氧化还原反应的是(填序号)
⑧⑨
⑧⑨
.(6)将8g 乙在足量丙中燃烧,所得气体D通入100mL 3.5mol?L-1的B溶液中,完全吸收后,溶液中的溶质及其物质的量分别为
0.1 5mol NaHSO3和0.1 mol Na2SO3
0.1 5mol NaHSO3和0.1 mol Na2SO3
;若同体积的气体D通入100mL 2.5mol?L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
.下表中列出了五种短周期元素A、B、C、D、E的信息,请推断后作答:
(1)写出A、B、C、D、E五种元素符号 、 、 、 、 .
(2)画出B的原子结构示意图: ;写出D元素最高价氧化物对应水化物的电子式: .
(3)盐X水溶液显 (选填“酸”、“碱”或“中”)性,用离子方程式解释其原因: .
(4)D2CA3的溶液与B的单质能发生氧化还原反应,其反应的离子方程式为 .
(5)已知E元素的某种氢化物Y与A2的摩尔质量相同,Y在常温下为液态,Y的化学式为 ,Y所含的化学键为 .
(a)极性键 (b)非极性键 (c)离子键.
查看习题详情和答案>>
| 元素 | 有关信息 |
| A | 元素主要化合价为-2,原子半径为0.074nm |
| B | 所在主族序数与所在周期序数之差为4,同周期主族元素中原子半径最小 |
| C | 原子半径为0.102nm,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应水化物,能按1:1电离出电子数相等(10个电子)的阴阳离子 |
| E | 原子半径为0.075nm,最高价氧化物对应水化物与其氢化物组成一种盐X |
(2)画出B的原子结构示意图:
(3)盐X水溶液显
(4)D2CA3的溶液与B的单质能发生氧化还原反应,其反应的离子方程式为
(5)已知E元素的某种氢化物Y与A2的摩尔质量相同,Y在常温下为液态,Y的化学式为
(a)极性键 (b)非极性键 (c)离子键.