摘要:下列说法中正确的是( ) A.C60气化和金刚石熔化克服的作用力相同 B.甲酸甲酯的熔点低于乙酸的熔点 C.氯化钠和氯化氢溶于水时.破坏的化学键都是离子键 D.分子晶体的熔沸点低.常温下均呈液态或气态
网址:http://m.1010jiajiao.com/timu3_id_327616[举报]
|
下列说法中正确的是 | |
| [ ] | |
A. |
C60气化和金刚石熔化克服的作用力相同 |
B. |
甲酸甲酯的熔点低于乙酸的熔点 |
C. |
氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 |
D. |
分子晶体的熔沸点低,常温下均呈液态或气态 |
|
下列说法中正确的是 | |
| [ ] | |
A. |
C60气化和金刚石熔化克服的作用力相同 |
B. |
甲酸甲酯的熔点低于乙酸的熔点 |
C. |
氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 |
D. |
分子晶体的熔沸点低,常温下均呈液态或气态 |
下列有关物质的性质的说法正确的是
[ ]
A.金刚石、C60都有较大的硬度和较高的熔点
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解
C.Cl2、SO2都可以使品红溶液褪色
D.镁、铁等金属在一定条件下与水反应都生成对应的氢氧化物和氢气
查看习题详情和答案>>
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解
C.Cl2、SO2都可以使品红溶液褪色
D.镁、铁等金属在一定条件下与水反应都生成对应的氢氧化物和氢气
 碳是形成化合物最多的元素.
碳是形成化合物最多的元素.(1)由碳元素参与形成的物质多为分子晶体,也有少数原子晶体.下列关于分子晶体和原子晶体的说法正确的是
A、完全由非金属元素形成的物质一定是分子晶体或原子晶体
B、分子晶体中分子之间一定存在范德华力
C、SiC具有极高的熔点和较大的硬度,SiC分子中除存在共价键外,还存在分子间作用力
D、金刚石是由碳元素形成的原子晶体,性质稳定,不与任何物质反应
(2)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子.C4分子结构如图所示.下列说法正确的是
A、C4属于一种新型的化合物 B、C4与P4(白磷)的晶体都属于分子晶体
C、C4气体分子内含有极性共价键 D、C4与C60互为同素异形
(3)与碳同主族元素锗为32号元素,与锗同周期,且未成对电子数与锗相同,电负性最大的元素的价电子排布式为
(4)邻硝基苯酚的熔点
(5)硼、碳、氮、氧是元素周期表第二周期相邻的四种元素.下列有关的四种化合
物中,键角最小的是
A、CO2 B、CF4 C、NF3 D、OF2
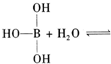
已知硼酸H3BO3为白色固体,溶于水显弱酸性,但它却是一元酸,可以用硼酸在水溶液中的电离平衡解释它是一元弱酸的原因.
请写出下面这个方程式右端的两种离子的表达式:
 查看习题详情和答案>>
查看习题详情和答案>>