摘要:在4L容器中加入18g水蒸气.28g一氧化碳.在t℃时发生如下反应: CO+H2O⇌CO2+H2 在最初5s内.一氧化碳的平均反应速率是0.02mol/.求: (1)5s末时.容器内一氧化碳和水蒸气的浓度. (2)5s末时.容器内二氧化碳的质量. 答案: (1)CO的浓度-0.02×5=0.15 H2O的浓度-0.02×5=0.15 (2)CO2的质量=0.02×5×4×44=17.6(g) 综合练习
网址:http://m.1010jiajiao.com/timu3_id_326852[举报]
在密闭容器中加入18.4gNaHCO3和NaOH固体混合物加热至250℃,经充分反应后排出气体,冷却称量剩余固体质量为16.6g,由此可推断
- A.两者都正好完全反应
- B.NaOH不足量
- C.NaHCO3质量为8.4g
- D.NaOH质量为4.0g
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
A.在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA
B.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA
C.1.0L的0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA
D.标准状况下,22.4L的CHCl3中含有的分子数为NA
查看习题详情和答案>>
(10分)将煤气化转化成合成气,然后通过一碳化工路线合成各种油品和石化产品是一碳化工的极为重要的领域,具有广阔的前景,在未来相当一段时期将成为一碳化工的主要领域。除去水蒸气后的水煤气含55~59%的H2,15~18%的CO,11~13%的CO2,少量的H2S、CH4,除去H 2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气,即可进行甲醇合成。
2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气,即可进行甲醇合成。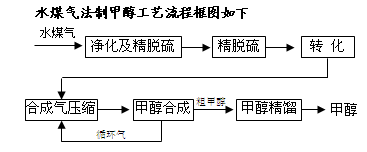
(1)制水煤气的主要化学反应方程式为:C(s)+H2O(g)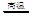 CO(g)+H2(g),此反应是吸热反应。①此反应的化学平衡常数表达式为 ;
CO(g)+H2(g),此反应是吸热反应。①此反应的化学平衡常数表达式为 ;
②下列能增大碳的转化率的 措施是 ;(填字母代号)
措施是 ;(填字母代号)
| A.加入C(s) | B.加入H2O(g) | C.升高温度 | D.增大压强 |
 CH3OH(g);ΔH =-90.8kJ·mol-1,T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g);ΔH =-90.8kJ·mol-1,T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:| 物质 | H2 | CO | CH3OH |
| 浓度/(mol·L-1) | 0.2 | 0.1 | 0.4[ |
②若加入CO、H2后,在T5℃反应10min达到平衡,c(H2)=0.4 mol·L-1,则该时间内反应速率v(CH3OH) = mol-1·(Lmin)-1。
(3)生产过程中,合成气要进行循环,其目的是
 。
查看习题详情和答案>>
。
查看习题详情和答案>>