摘要:在可逆反应中混合物各成分的浓度比一定等于各物质分子系数比的是( ). A.起始浓度 B.转化浓度 C.平衡浓度 D.都不等
网址:http://m.1010jiajiao.com/timu3_id_326823[举报]
可逆反应N2+3H2?2NH3是工业上合成氨的重要反应.
(1)根据图1请写出合成氨的热化学方程式
(2)图1中虚线部分是通过改变化学反应条件是
(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率随时间的关系,其中表示平衡混合物中NH3的含量最高的时间段是
(4)在一定温度压强下,下列各项能作为判断该反应达到化学平衡状态的依据是
a.单位时间内生成2n molNH3的同时生成n molN2 b.容器内压强不再改变
c.容器内N2、H2、NH3的浓度之比为1:3:2 d.混合气体的密度不再改变
e.混合气体的平均相对分子质量不再改变 f.2v正(H2)=3v正(NH3)
(5)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为
.若此时再向该容器中投入a mol H2、amol N2和amol NH3,则此时化学平衡
查看习题详情和答案>>

(1)根据图1请写出合成氨的热化学方程式
N2(g)+3H2(g)?2NH3(g)△H=-2(E3-E1)kg/mol
N2(g)+3H2(g)?2NH3(g)△H=-2(E3-E1)kg/mol
(热量用E1、E2或E3表示)(2)图1中虚线部分是通过改变化学反应条件是
使用催化剂
使用催化剂
,请解释原因因为催化剂能改变反应的路径,使发生反应所需的活化能降低
因为催化剂能改变反应的路径,使发生反应所需的活化能降低
.(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率随时间的关系,其中表示平衡混合物中NH3的含量最高的时间段是
t0-t1
t0-t1
(用含t符号表示)(4)在一定温度压强下,下列各项能作为判断该反应达到化学平衡状态的依据是
ade
ade
(填字母).a.单位时间内生成2n molNH3的同时生成n molN2 b.容器内压强不再改变
c.容器内N2、H2、NH3的浓度之比为1:3:2 d.混合气体的密度不再改变
e.混合气体的平均相对分子质量不再改变 f.2v正(H2)=3v正(NH3)
(5)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为
| 16 |
| a2 |
| 16 |
| a2 |
正向
正向
移动(填“正向”、“逆向”或“不”)可逆反应2NH3 N2+3H2在密闭容器中进行,达到平衡状态的标志是( )
N2+3H2在密闭容器中进行,达到平衡状态的标志是( )
①单位时间内生成n mol N2的同时生成2n mol NH3 ②单位时间内生成n mol N2的同时生成3n mol H2 ③用NH3、N2、H2的物质的量浓度变化表示的反应速率之比为2∶1∶3 ④各气体的浓度不再改变 ⑤混合气体的平均相对分子质量不再改变?
 N2+3H2在密闭容器中进行,达到平衡状态的标志是( )
N2+3H2在密闭容器中进行,达到平衡状态的标志是( )①单位时间内生成n mol N2的同时生成2n mol NH3 ②单位时间内生成n mol N2的同时生成3n mol H2 ③用NH3、N2、H2的物质的量浓度变化表示的反应速率之比为2∶1∶3 ④各气体的浓度不再改变 ⑤混合气体的平均相对分子质量不再改变?
| A.①④⑤ | B.②③⑤? | C.①③④ | D.①②③④⑤? |
可逆反应2NH3 N2+3H2在密闭容器中进行,达到平衡状态的标志是( )
N2+3H2在密闭容器中进行,达到平衡状态的标志是( )
①单位时间内生成n mol N2的同时生成2n mol NH3 ②单位时间内生成n mol N2的同时生成3n mol H2 ③用NH3、N2、H2的物质的量浓度变化表示的反应速率之比为2∶1∶3 ④各气体的浓度不再改变 ⑤混合气体的平均相对分子质量不再改变?
| A.①④⑤ | B.②③⑤? | C.①③④ | D.①②③④⑤? |
在![]() 的可逆反应中
,下列状态中达到了化学平衡状态的是
的可逆反应中
,下列状态中达到了化学平衡状态的是
[
]A
.氮气、氢气和氨气的分子数比为1∶3∶2B
.氮气、氢气、氨气的浓度不再变化的状态C
.氮气、氢气的分子数与生成氨的分子数相等的状态D
.反应混合物中各组成成分的摩尔分数不再随时间的延长而改变的状态 查看习题详情和答案>>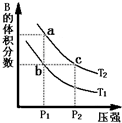 对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.
对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.(1)根据曲线图,分析下列说法正确的是
BC
BC
(填字母).A.a、c两点的反应速率:a>c
B.由状态b到状态a,可以通过加热的方法
C.b、c两点A气体的转化率相等
(2)上述反应在密闭容器(定容)中进行,达到平衡状态的标志是
BE
BE
(填字母).A.单位时间内生成n mol A的同时分解2n molB
B.两种气体的体积分数不再改变
C.v正(A)=2v逆(B)
D.混合气体的密度不再发生变化
E.混合气体的压强不再发生变化
(3)若上述反应达平衡时,B气体的平衡浓度为0.1mol?L-1,通过减小体积来增大体系的压强(温度保持不变),重新达平衡后,B气体的平衡浓度
>
>
0.1mol?L-1(填“>”、“<”或“=”).(4)在100℃时,将0.40mol的B气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表的数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(B)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(A)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
0.000875mol/(L?s)
0.000875mol/(L?s)
;②上表中n3
=
=
n4(填“>”、“<”或“=”),反应A(g)?2B(g)在100℃时的平衡常数K的值为0.36
0.36
,升高温度后,反应2B(g)?A(g)的平衡常数K的值减小
减小
(填“增大”、“减小”或“不变”);③若在相同情况下最初向该容器中充入的是A气体,要达到上述同样的平衡状态,A气体的起始浓度为
0.1
0.1
mol?L-1.