网址:http://m.1010jiajiao.com/timu3_id_326235[举报]
请回答下列问题:
(1)根据以上数据,写出C(石墨,s)与水蒸气反应的热化学反应方程式:
(2)比较反应热数据可知,1mol CO(g)和1mol H2(g)完全燃烧放出的热量之和比1mol C(石墨,s)完全燃烧放出的热量多.甲同学据此认为“煤转化为水煤气可以使燃烧放出更多的热量”;乙同学根据盖斯定律作出如图1所示循环图,并据此认为“煤转化为水煤气后再燃烧放出的热量与煤直接燃烧放出的热量相等”.
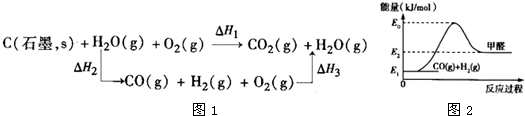
请评价甲、乙两同学的观点,正确的是
(3)人们把拆开1mol化学键所吸收的能量看成该化学键的键能.已知:石墨、O2分子中化学键的键能分别是460.7kJ/mol、497kJ/mol,则C=O键的键能为
(4)炼铁高炉中可将煤转化为CO再还原铁的氧化物,已知炼铁过程中有下列热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8kJ/mol
②Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.4kJ/mol
由FeO固体得到Fe固体和CO2气体时对应的△H约为
(5)水煤气也是重要的有机化工原料.CO和H2在一定条件下可以合成甲醛,能满足“绿色化学”的要求,完全利用原料中的原子,实现零排放.该反应过程的能量变化如图2所示.该反应属于
| ||
②C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g);△H=-393.5kJ?mol-1
H2(g)+
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
请回答:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学反应方程式:
(2)比较反应热数据可知,1mol CO(g)和1mol H2(g)完全燃烧放出的热量之和比1mol C(s)完全燃烧放出的热量多.甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律做出下列循环图:
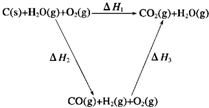
并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”.
请分析:甲、乙两同学观点正确的是
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点
(4)已知热化学方程式:
Mg(OH)2(s)=MgO(s)+H2O(g)△H1=+81.5kJ?mol-1
Al(OH)3(s)=
| 1 |
| 2 |
| 3 |
| 2 |
①Mg(OH)2和Al(OH)3起阻燃作用的主要原因是
②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
党的十七大报告指出:“加强能源资源节约和生态环境保护,增强可持续发展能力,坚持节约资源和保护环境的基本国策,发展环保产业.”
(1)下列有关做法不符合上述要求的是________.
A.将煤液化、气化,提高燃料的燃烧效率
B.安装汽车尾气催化转化装置,使之反应:4CO+2NO2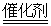 4CO2+N2
4CO2+N2
C.大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃烧电池汽车
D.在水力发电、火力发电、核能发电和风力发电中要大力发展火力发电
(2)将煤转化为水煤气的主要化学反应为
C(s)+H2O(g) CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为:
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol ①
H2(g)+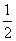 O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②
O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②
CO(g)+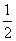 O2(g)===CO2(g)
ΔH=-283.0 kJ/mol
③
O2(g)===CO2(g)
ΔH=-283.0 kJ/mol
③
请回答:
①根据以上数据,写出C(s)与H2O(g)反应的热化学方程式:_____________________________________.
②水煤气不仅是优良的气体燃料,也是重要的有机化工原料,CO和H2在一定条件下可以合成:a.甲醇;b.甲醛;c.甲酸;d.乙酸.试分析当CO和H2按1∶1的体积比混合反应,合成上述________(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放.
查看习题详情和答案>>
C(s)+O2(g)====CO2(g) ΔH=-393.5 kJ·mol-1 (1)
H2(g)+![]() O2(g)====H2O(g) ΔH=-242.0 kJ·mol-1 (2)
O2(g)====H2O(g) ΔH=-242.0 kJ·mol-1 (2)
CO(g)+12O2(g)====CO2(g) ΔH=-283.0 kJ·mol-1 (3)
请回答:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学方程式:___________________。

(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比1 mol C(s)完全燃烧放出的热量多。甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律作出如上循环图:
并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。
请分析:甲、乙两同学观点正确的是____________(填“甲”或“乙”);判断的理由是__________。
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点______________。
(4)水煤气不仅是优良的气体燃料,也是重要的有机化工原料。CO和H2在一定条件下可以合成:①甲醇 ②甲醛 ③甲酸 ④乙酸。试分析当CO和H2按1:1的体积比混合反应,合成上述______________(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放。
查看习题详情和答案>>党的十七大报告指出:“加强能源资源节约和生态环境保护,增强可持续发展能力,坚持节约资源和保护环境的基本国策,发展环保产业.”
(1)下列有关做法不符合上述要求的是________.
| A.将煤液化、气化,提高燃料的燃烧效率 |
B.安装汽车尾气催化转化装置,使之反应:4CO+2NO2 4CO2+N2 4CO2+N2 |
| C.大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃烧电池汽车 |
| D.在水力发电、火力发电、核能发电和风力发电中要大力发展火力发电 |
C(s)+H2O(g)
 CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、H2(g)和CO(g)完全燃烧的热化学方程式为:C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol ①
H2(g)+
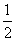 O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②
O2(g)===H2O(g) ΔH=-242.0 kJ/mol ②CO(g)+
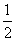 O2(g)===CO2(g) ΔH=-283.0 kJ/mol ③
O2(g)===CO2(g) ΔH=-283.0 kJ/mol ③请回答:
①根据以上数据,写出C(s)与H2O(g)反应的热化学方程式:_____________________________________.
②水煤气不仅是优良的气体燃料,也是重要的有机化工原料,CO和H2在一定条件下可以合成:a.甲醇;b.甲醛;c.甲酸;d.乙酸.试分析当CO和H2按1∶1的体积比混合反应,合成上述________(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放. 查看习题详情和答案>>