摘要:24. Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢.有时还很不完全.测定反应热很困难.现在可根据盖斯定律进行计算. 已知:P4+5O2(g)= P4O10(s) △H=-2983.2kJ·mol-1 ① P+O2(g)=P4O10(s) △H=-738.5kJ·mol-1 ② (1)试写出白磷转化为红磷的热化学方程式 . (2)由热化学方程式来看.更稳定的磷的同素异形体是 . Ⅱ2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= -99kJ·mol-1.请回答下列问题: (1)图中E的大小对该反应的反应热有无影响? .(填“有影响 或“无影响 ).该反应通常用V2O5作催化剂.加V2O5会使图中B点升高还是降低? (2)图中△H= kJ·mol-1..
网址:http://m.1010jiajiao.com/timu3_id_325778[举报]
 Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.
Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.已知:P4(s,白磷)+5O2(g)=P4O10(s)△H=-2983.2kJ?mol-1 ①
P(s,红磷)+
| 5 |
| 4 |
| 1 |
| 4 |
(1)试写出白磷转化为红磷的热化学方程式
(2)由热化学方程式来看,更稳定的磷的同素异形体是
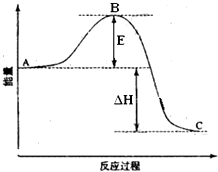
Ⅱ(6分)2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
(1)图中E的大小对该反应的反应热有无影响?
(2)图中△H=
(4分)同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算。
已知:P4(固体.白磷)+5O2(气体)= P4O10(固体) △H=-2983.2kJ·mol-1 ①
P(固体.红磷)+O2(气体)=P4O10(固体) △H=-738.5kJ·mol-1 ②
⑴ 由热化学方程式来看,更稳定的磷的同素异形体是
⑵ 试写出白磷转化为红磷的热化学方程式
查看习题详情和答案>>
(3分)同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算。
已知:
(1)由热化学方程式来看,更稳定的磷的同素异形体是_____________________________。
(2)试写出白磷转化为红磷的热化学方程式___________________________________。
查看习题详情和答案>>