网址:http://m.1010jiajiao.com/timu3_id_325544[举报]
已知R、W、X、Y、Z是周期表中前四凰期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X2+与W2-具有相同的电子层结构;Y元素原子的3p能级处于半充满状态;Z+的电子层都充满电子.请回答下列问题:
(1)写出Z的基态原子的外围电子排布式 .
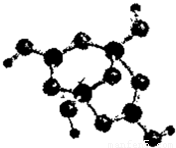
(2)R的某种钠盐晶体,其阴离子Am-(含R、W、氢三种元素)的球棍模型如图所示:在Am-中,R原子轨道杂化类型有 ;m= .(填数字)
(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X2+的配位原子所构成的立体几何构型为 .
(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH3)4]SO4,下列说法正确的是
A.[Z(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
D.在[Z(NH3)4]SO4中Z2+给出孤对电子,NH3提供空轨道
C.[Z(NH3)4]SO4组成元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为四面体
(5)固体YCl5的结构实际上是Ycl4+和YCl6-构成的离子晶体,其晶体结构与CsCl相似.若晶胞边长为apm,则晶胞的密度为 g?cm-3.
 查看习题详情和答案>>
查看习题详情和答案>>
 (2013?辽宁一模)[化学--选修3物质结构与性质]
(2013?辽宁一模)[化学--选修3物质结构与性质]已知R、W、X、Y、Z是周期表中前四凰期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X2+与W2-具有相同的电子层结构;Y元素原子的3p能级处于半充满状态;Z+的电子层都充满电子.请回答下列问题:
(1)写出Z的基态原子的外围电子排布式
(2)R的某种钠盐晶体,其阴离子Am-(含R、W、氢三种元素)的球棍模型如图所示:在Am-中,R原子轨道杂化类型有
(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X2+的配位原子所构成的立体几何构型为
(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH3)4]SO4,下列说法正确的是
A.[Z(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(NH3)4]SO4中Z2+给出孤对电子,NH3提供空轨道
C.[Z(NH3)4]SO4组成元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为四面体
(5)固体YCl5的结构实际上是Ycl4+和YCl6-构成的离子晶体,其晶体结构与CsCl相似.若晶胞边长为apm,则晶胞的密度为
| 417×1030 |
| a3NA |
| 417×1030 |
| a3NA |
有X、Y、Z、Q、M、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层.M、N原子的价层电子构型为nS1,其电离能数据如下表:
| M | N | |
| 第一电离能(kJ/mol) | 495.8 | 418.8 |
(1)Z元素原子的价层电子的轨道表示式为:


(2)由X、Y形成的Y2X2分子中,含有
(3)比较ME、NE的熔点高低并说明理由

(4)Y、Z、Q的第一电离能由小到大的顺序为
(5)YQ2中心原子的杂化方式为


(6)GE的晶胞结构如图所示,阴离子周围最近的阳离子有
| 4×99.5g/mol |
| ag/cm3×6.02×1023mol-1 |
| 4×99.5g/mol |
| ag/cm3×6.02×1023mol-1 |
[选修一物质结构与性质] (15分)
有X、Y、Z、Q、M 、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层。M、N原子的价层电子构型为nS1,其电离能数据如下表:
|
| M | N |
| 第一电离能(kJ/mol) | 495.8 | 418.8 |
回答下列问题:
(1)Z元素原子的价层电子的轨道表示式为: ;
(2)由X、Y形成的Y2X2分子中,含有 个键, 个
键:
(3)比较ME、NE的熔点高低并说明理由 。
(4)Y、Z、Q的第一电离能由小到大的顺序为 。(用元素符号回答)
(5)YQ2中心原子的杂化方式为___________,有一种与YQ2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式________________。
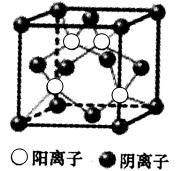
(6)GE的晶胞结构如图所示,阴离子周围最近的阳离子有 个;GE晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出计算式)。
查看习题详情和答案>>
[选修一物质结构与性质] (15分)
有X、Y、Z、Q、M 、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层。M、N原子的价层电子构型为nS1,其电离能数据如下表:
| | M | N |
| 第一电离能(kJ/mol) | 495.8 | 418.8 |
(1)Z元素原子的价层电子的轨道表示式为: ;
(2)由X、Y形成的Y2X2分子中,含有 个
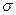 键, 个
键, 个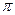 键:
键:(3)比较ME、NE的熔点高低并说明理由 。
(4)Y、Z、Q的第一电离能由小到大的顺序为 。(用元素符号回答)
(5)YQ2中心原子的杂化方式为___________,有一种与YQ2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式________________。
(6)GE的晶胞结构如图所示,阴离子周围最近的阳离子有 个;GE晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出计算式)。
 查看习题详情和答案>>
查看习题详情和答案>>