摘要:25.有A.B.C.D四种主族元素.其中A元素和B元素的原子都有1个未成对电子.A+比B-少一个电子层.B原子得一个电子填入3p轨道后.3p轨道已充满,C原子的p轨道中有3个未成对电子.其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大,D的最高化合价和最低化合价的代数和为4.其最高价氧化物中含D的质量分数为40%.且其核内质子数等于中子数.R是由A.D两元素形成的离子化合物.其中A+与D2-离子数之比为2:1. 请回答下列问题: (1)A元素形成的晶体属于 晶体.其熔点比同周期的金属元素单质的要低.这是因为 . (2)B- 的电子排布式为 .在CB3分子中C元素原子的原子轨道发生的是 杂化. (3)C的氢化物的空间构型为 ,C的氢化物的沸点比其相邻周期元素的沸点 .原因是: (4)B元素的电负性 D元素的电负性(填“> .“< 或“= ),用一个化学方程式说明B.D两元素形成的单质的氧化性强弱: . (5)用电子式表示化合物R的形成过程: .
网址:http://m.1010jiajiao.com/timu3_id_325528[举报]
 有A、B、C、D四种短周期元素,其原子序数依次增大.A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物.回答下列问题.
有A、B、C、D四种短周期元素,其原子序数依次增大.A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物.回答下列问题.(1)A2B2的电子式为


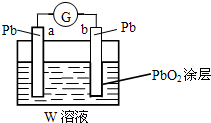
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示).在b电极上发生的反应可表示为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为
Pb-2e-+SO42-=PbSO4
Pb-2e-+SO42-=PbSO4
.(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期.该元素可与D形成ED2和ED3两种化合物.将E的单质浸入ED3溶液中(如图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为
Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
.
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池,则在该原电池工作时,石墨一极发生的反应可以表示为
2Fe3++2e-=2Fe2+
2Fe3++2e-=2Fe2+
.比较甲、乙两图,说明石墨除形成闭合回路外所起的作用是使还原反应和氧化反应在电解质溶液中的不同区域内发生
使还原反应和氧化反应在电解质溶液中的不同区域内发生
.有A、B、C、D四种短周期的主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅占据一种原子轨道,也是宇宙中最丰富的元素,B元素原子的核外p轨道电子数比s轨道电子数少1,C为金属元素且原子核外p轨道电子数和s轨道电子数相等;D元素的原子核外所有p轨道全满或半满.
(1)写出四种元素的元素符号:A
(2)写出D元素基态原子的外围电子排布式:
(3)写出B、C两种元素的单质在一定条件下反应的化学方程式
(4)写出C元素形成的氯化物的电子式:
 .
.
查看习题详情和答案>>
(1)写出四种元素的元素符号:A
H
H
;BN
N
;CMg
Mg
;DP
P
.(2)写出D元素基态原子的外围电子排布式:
3s23p3
3s23p3
;(3)写出B、C两种元素的单质在一定条件下反应的化学方程式
3Mg+N2
Mg3N2
| ||
3Mg+N2
Mg3N2
.
| ||
(4)写出C元素形成的氯化物的电子式:


有A、B、C、D四种短周期元素,它们的原子序数依次增大,其中A与D同主族,且最外层只有1个电子;B原子的最外层电子数是奇数,其单质在常温下为难于液化的气体;C原子最外层电子数是次外层电子数的3倍.E与B同主族,且原子有六个电子层.试回答下列问题:
(1)B的气态氢化物的空间构型为 .
(2)由C、D两元素按原子个数比为1:1形成的化合物的电子式为 .
(3)氢键通常用X-H…Y来表示,其中X、Y为N、O、F,“-”表示共价键,“…”表示形成的氢键,则BA3与A2C的混合物中所形成的氢键可表示为(任写一种) .
(4)由A、B、C三元素形成的常见盐的水溶液呈酸性,其原因是(用离子反应方程式表示) ,该溶液中离子浓度由大到小的顺序为 .
(5)DEC3微溶于水,其氧化性大于KMnO4,将DEC3固体投入浓HCl中可形成E的低价氯化物,同时产生黄绿色气体,其离子反应方程式为 .
查看习题详情和答案>>
(1)B的气态氢化物的空间构型为
(2)由C、D两元素按原子个数比为1:1形成的化合物的电子式为
(3)氢键通常用X-H…Y来表示,其中X、Y为N、O、F,“-”表示共价键,“…”表示形成的氢键,则BA3与A2C的混合物中所形成的氢键可表示为(任写一种)
(4)由A、B、C三元素形成的常见盐的水溶液呈酸性,其原因是(用离子反应方程式表示)
(5)DEC3微溶于水,其氧化性大于KMnO4,将DEC3固体投入浓HCl中可形成E的低价氯化物,同时产生黄绿色气体,其离子反应方程式为
有A、B、C、D四种元素。已知:(1)它们均为周期表中前20号元素,C、D在同一周期,A、B在同一主族;(2)它们可以组成化合物B2C 2、A2C 、DC2等;(3)B的阳离子与C的阴离子的核外电子排布相同;(4)B2C 2同A2C 或DC2反应都生成C2的气体,B与A2C 反应产生气体A2,A2与气体C2按体积2∶1混合后点燃能发生爆炸,其产物是一种无色、无味的液体(在常温下)。请回答下列问题:
(1)写出A、B、C、D四种元素的符号:A__________、B__________、C__________、D__________。
(2)在B
有A、B、C、D四种元素,已知:
①均为周期表中前20号元素,A、B在同一主族,C、D在同一周期;
②相互间可组成B2C2、A2C、D C2等化合物;
③B的阳离子与C的阴离子核外电子排布相同;
④B2C2同A2C或者D C2反应都生成气体C2,B单质与A2C反应生成气体A2,气体A2与C2按照体积比2∶1混合,点火爆炸,完全化合成常温下无色、无味的液体A2C,请完成下面的问题。
(1)写出四种元素的符号:A_________;B_________;C_________;D_________。
(2)BCA的电子式为_________,其化学键的类型为__________________。
(3)B2C2与DC2反应的化学方程式为____________________________________________。
(4)B2C2与A2C的反应的化学方程式为__________________________________________。
查看习题详情和答案>>