摘要:15.在25℃时.用石墨电极电解2.0L2.5mol/LCuSO4溶液.如有0.20 mol电子发生转移.请回答下列问题: (1)阴极发生 反应.电极反应式为 , (2) 阳极发生 反应.电极反应式为 , (3)电解后得到的铜的质量是 .得到氧气的体积是 .溶液的pH是 , (4)如用等质量的两块铜片代替石墨做电极.电解后两铜片的质量相差 ,电解液的pH . 拓展提高
网址:http://m.1010jiajiao.com/timu3_id_324569[举报]
(2013?济南二模)硫元素的化合物在生产、生活中有着广泛的应用.
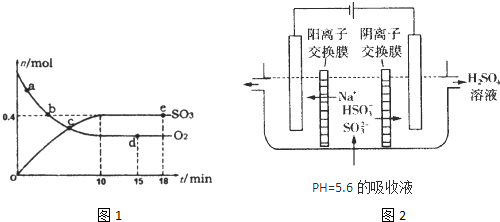
(1)400℃,1.01×105Pa下,容积为1.0L的密闭容器中充入0.5molSO2,(g)和0.3molO2 (g),发生2SO2(g)+O2(g)?2SO3(g)△H=-198kJ?mol-1反应中n(SO3)和n(O2)随时间变化的关系如图1所示.反应的平衡常数K=
A.a点时刻的正反应速率比b点时刻的大
B.c点时刻反应达到平衡状态
C.d点和e点时刻的c(O2)相同
D.若500℃,1.01×105Pa下,反应达到平衡时,n( SO3)比图中e点时刻的值大
(2)用NaOH溶液吸收工业废气中的SO2,当吸收液失去吸收能力时,25℃时测得溶液的pH=5.6,溶液中Na+,H+,SHO3-,SO32-离子的浓度由大到小的顺序是
(3)可通过电解法使(2)中的吸收液再生而循环利用(电极均为石墨电极),其工作示意图如图2:HSO3-在阳极室反应的电极反应式为
查看习题详情和答案>>
(1)400℃,1.01×105Pa下,容积为1.0L的密闭容器中充入0.5molSO2,(g)和0.3molO2 (g),发生2SO2(g)+O2(g)?2SO3(g)△H=-198kJ?mol-1反应中n(SO3)和n(O2)随时间变化的关系如图1所示.反应的平衡常数K=
160
160
;0到10min内用SO2:表示的平均反应速率0.04mol/(L?min)
0.04mol/(L?min)
.更具图1中信息,判断下列叙述中正确的是AC
AC
(填序号).
A.a点时刻的正反应速率比b点时刻的大
B.c点时刻反应达到平衡状态
C.d点和e点时刻的c(O2)相同
D.若500℃,1.01×105Pa下,反应达到平衡时,n( SO3)比图中e点时刻的值大
(2)用NaOH溶液吸收工业废气中的SO2,当吸收液失去吸收能力时,25℃时测得溶液的pH=5.6,溶液中Na+,H+,SHO3-,SO32-离子的浓度由大到小的顺序是
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
(3)可通过电解法使(2)中的吸收液再生而循环利用(电极均为石墨电极),其工作示意图如图2:HSO3-在阳极室反应的电极反应式为
HSO3-+H2O-2e-=SO42-+3H+
HSO3-+H2O-2e-=SO42-+3H+
.阴极室的产物H2、NaOH
H2、NaOH
.硫元素的化合物在生产、生活中有着广泛的应用。
(1)400℃,1.01× Pa下,容积为1.0L的密闭容器中充入0.5molSO2,
(g)和0.3 molO2 (g),发生反应2SO2(g)+O2(g)
Pa下,容积为1.0L的密闭容器中充入0.5molSO2,
(g)和0.3 molO2 (g),发生反应2SO2(g)+O2(g) 2SO3(g)
△H=-198kJ/mol。反应中n(SO3)和n(O2)随时间变化的关系如右图所示
2SO3(g)
△H=-198kJ/mol。反应中n(SO3)和n(O2)随时间变化的关系如右图所示 。反应的平衡常数K=_______;0到10 min内用SO2表示的平均反应速率_________。根据图中信息,判断下列叙述中正确的是_____(填序号)。
。反应的平衡常数K=_______;0到10 min内用SO2表示的平均反应速率_________。根据图中信息,判断下列叙述中正确的是_____(填序号)。
A.a点时刻的正反应速率比b点时刻的大
B.c点时刻反应达到平衡状态
C.d点和e点时刻的c(O2)相同
D.若5 00℃,1.01×105Pa下,反应达到平衡时,n( SO3) 比图中e点时刻的值大
(2)用NaOH溶液吸收工业废气中的SO2,当吸收液失去吸收能力时,25℃时测得溶液的pH=5.6,溶液中Na+,H+, HSO3-,SO32-离子的浓度由大到小的顺序是__________________。
(3)可通过电解法使(2)中的吸收液再生而循环利用(电极均为石墨电极),其工作示意图如下:

HSO3-在阳极室反应的电极反应式为________________________,阴极室的产物_________________。
查看习题详情和答案>>