网址:http://m.1010jiajiao.com/timu3_id_324245[举报]
(1)甲的化学式为RClx。
①若甲为某短周期金属元素的氯化物,甲中含有的金属元素的原子半径在同周期金属元素中最小,其阳离子与氖原子有相同的电子层结构。则甲中含有的金属元素是________;
②若甲为某金属元素的棕色氯化物,将该氯化物水溶液加热蒸干并灼烧,得到的氧化物为红棕色粉末,则甲的化学式为________,甲中含有的金属元素在周期表中的位置为________,
③将上述两种金属中活泼性强的金属与另一种金属的最高价氧化物混合,引燃后可发生剧烈反应,其化学方程式为________,引燃该反应的实验操作是________。
(2)若甲、乙、丙、丁为单质或化合物,均含有某短周期中的同一种元素,常温下甲为气体,将甲通入常温下的KOH溶液中得到乙和丙,丙的水溶液具有强氧化性。
①电解乙溶液得到甲,该反应的化学方程式为__________;
②在一定条件下1 mol甲与2 mol KOH在溶液中反应得到乙和丁,n(乙):n(丁)=5:1,该反应的离子方程式为___________________。
查看习题详情和答案>>(13分)已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
(1)若甲的化学式为RCl3,其溶液在加热蒸于并灼烧时可发生如下反应:
a.甲+H2O![]() 乙十丙 b.乙
乙十丙 b.乙![]() 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则该金属在周期表中的位置是: 。
②若甲为某短周期金属元素的氯化物,则甲发生a反应的化学方程式为:____。
③将以上两种金属单质用导线连接,插入一个盛有NaOH溶液的烧杯中构成原电池,则负极发生的电极反应为 。
(2)若甲、乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲十乙![]() 丙。则:
丙。则:
①甲的结构式为 。
②写出上述反应的化学方程式 。
③写出在200mL 2mol/L的NaOH溶液中通入6.72L(标准状况)的气体甲发生完全反应的总离子方程式 。
查看习题详情和答案>>
(13分)已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
(1)若甲的化学式为RCl3,其溶液在加热蒸于并灼烧时可发生如下反应:
a.甲+H2O 乙十丙 b.乙
乙十丙 b.乙 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则该金属在周期表中的位置是: 。
②若甲为某短周期金属元素的氯化物,则甲发生a反应的化学方程式为:____。
③将以上两种金属单质用导线连接,插入一个盛有NaOH溶液的烧杯中构成原电池,则负极发生的电极反应为 。
(2)若甲、乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲十乙 丙。则:
丙。则:
①甲的结构式为 。
②写出上述反应的化学方程式 。
③写出在200mL 2mol/L的NaOH溶液中通入6.72L(标准状况)的气体甲发生完全反应的总离子方程式 。
查看习题详情和答案>>
已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
Ⅰ.若甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
a.甲+H2O 乙+丙 b.乙
乙+丙 b.乙 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则甲发生a反应的化学方程式为:
②若甲为某短周期金属元素的氯化物,则该金属在周期表中的位置是: ;
若向30 mL 1 mol/L的甲的溶液中逐渐加入浓度为4 mol/L的NaOH溶液,若产生0.78 g白色沉淀,则加入的NaOH溶液的体积可能为 (选填编号).
| A.3 mL | B.7.5 mL | C.15 mL | D.27.5 mL |
Ⅱ.若甲,乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲+乙
 丙。则:
丙。则:①写出上述反应的化学方程式 。
②0.5 mol气体甲与足量的过氧化钠反应,转移电子的数目为
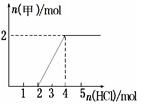
③将一定量气体甲通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(甲)的关系如图所示,溶液A中各离子浓度由大到小的顺序为 。
 查看习题详情和答案>>
查看习题详情和答案>>
已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
(1)若甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
a.甲+H2O![]() 乙+丙 b.乙
乙+丙 b.乙![]() 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红
棕色粉末,则该金属在周期表中的位置是 。
②若甲为某短周期金属元素的氯化物,则甲发生a反应的化学方程式为
_ 。
③将以上两种金属单质用导线连接,插入一个盛有NaOH溶液的烧杯中构成原电池,
则负极发生的电极反应为 。
(2)若甲,乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单
质,甲和丙均为气态化合物,且可发生反应:甲+乙![]() 丙。
丙。
则:①甲的结构式为 。
②写出上述反应的化学方程式 。
③写出在200mL 2mol/L的NaOH溶液中通入6.72L(标准状况)的气体甲发生
完全反应的总离子方程式 。
查看习题详情和答案>>