摘要:1.降低,小于,增大体积使CO2压强减小.平衡向右移动.因正反应吸热.故使体系温度降低.重新平衡时.CO2压强必小于850℃时平衡压强
网址:http://m.1010jiajiao.com/timu3_id_323330[举报]
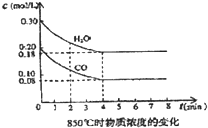 在一体积为10L的容器中,通入一定量的CO和H2O,在85℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-Q kJ/mol CO和H2O浓度变化如图,则
在一体积为10L的容器中,通入一定量的CO和H2O,在85℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-Q kJ/mol CO和H2O浓度变化如图,则(1)0-4min的平均反应速率v(CO)=
0.003
0.003
mol/(L?min)(2)下列能说明反应达到平衡状态的是
ce
ce
.a、每消耗1mol CO2的同时生成l molH2O b、体系压强保持不变
c、v正(CO)=v逆(CO2) d、容器中混合气体的密度保持不变
e、混合气体中H2O的体积分数保持不变 f、CO2和H2的体积比保持不变
t1℃时物质浓度(mol/L)的变化
| 时间 | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3min-4min之间反应处于
平衡
平衡
状态;C1数值大于
大于
0.08mol/L(填大于、小于或等于).②反应在4min-5min之间,平衡向逆方向移动,可能的原因是
d
d
(单选),表中5min-6min之间数值发生变化,可能的原因是a
a
(单选).a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.
在一体积为10L的容器中,通入一定量的CO和H2O,在85℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-Q kJ/mol CO和H2O浓度变化如图,则
(1)0-4min的平均反应速率v(CO)=______mol/(L?min)
(2)下列能说明反应达到平衡状态的是______.
a、每消耗1mol CO2的同时生成l molH2O b、体系压强保持不变
c、v正(CO)=v逆(CO2) d、容器中混合气体的密度保持不变
e、混合气体中H2O的体积分数保持不变 f、CO2和H2的体积比保持不变
t1℃时物质浓度(mol/L)的变化
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min-4min之间反应处于______状态;C1数值______0.08mol/L(填大于、小于或等于).
②反应在4min-5min之间,平衡向逆方向移动,可能的原因是______(单选),表中5min-6min之间数值发生变化,可能的原因是______(单选).
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.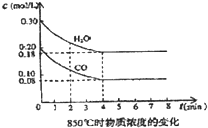
查看习题详情和答案>>
(1)0-4min的平均反应速率v(CO)=______mol/(L?min)
(2)下列能说明反应达到平衡状态的是______.
a、每消耗1mol CO2的同时生成l molH2O b、体系压强保持不变
c、v正(CO)=v逆(CO2) d、容器中混合气体的密度保持不变
e、混合气体中H2O的体积分数保持不变 f、CO2和H2的体积比保持不变
t1℃时物质浓度(mol/L)的变化
| 时间 | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3min-4min之间反应处于______状态;C1数值______0.08mol/L(填大于、小于或等于).
②反应在4min-5min之间,平衡向逆方向移动,可能的原因是______(单选),表中5min-6min之间数值发生变化,可能的原因是______(单选).
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.

如何降低大气中CO2含量及有效地开发利用CO2是当前科学家研究的重要课题。
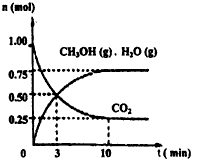
(1)科学家用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2L的密闭容器中,充入1molCO2和3.25molH2在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间变化如图所示:
①从反应开始到3min,氢气的平均反应速率v(H2)=__________;
②下列措施中一定能使CO2的转化率增大的是_________。
A.在原容器中再充入1molCO2 B.在原容器中再充入1molH2 C.在原容器中充入1mol氦气
D.使用更有效的催化剂 E.缩小容器的容积 F.将水蒸气从体系中分离
(2)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3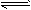
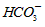 +H+的电离平衡常数 K=__________ 。(已知:10-5.6=2.5×10-6)
+H+的电离平衡常数 K=__________ 。(已知:10-5.6=2.5×10-6)
(3)科学家还利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) ΔH=a kJ/mol,在一定压强下,测得该反应的实验数据如下表。请根据表中数据分析
CH3CH2OH(g)+3H2O(g) ΔH=a kJ/mol,在一定压强下,测得该反应的实验数据如下表。请根据表中数据分析
①从反应开始到3min,氢气的平均反应速率v(H2)=__________;
②下列措施中一定能使CO2的转化率增大的是_________。
A.在原容器中再充入1molCO2 B.在原容器中再充入1molH2 C.在原容器中充入1mol氦气
D.使用更有效的催化剂 E.缩小容器的容积 F.将水蒸气从体系中分离
(2)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3
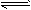
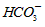 +H+的电离平衡常数 K=__________ 。(已知:10-5.6=2.5×10-6)
+H+的电离平衡常数 K=__________ 。(已知:10-5.6=2.5×10-6)(3)科学家还利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) ΔH=a kJ/mol,在一定压强下,测得该反应的实验数据如下表。请根据表中数据分析
CH3CH2OH(g)+3H2O(g) ΔH=a kJ/mol,在一定压强下,测得该反应的实验数据如下表。请根据表中数据分析
①上述反应的a________0(填“大于”或“小于”)。
②恒温下,向反应体系中加入固体催化剂,则反应产生的热量________(填“增大”、“减小”或“不变)。
③增大的值,则生成乙醇的物质的量____(填“增大”、“减小”、“不变”或“不能确定”)。
查看习题详情和答案>>
②恒温下,向反应体系中加入固体催化剂,则反应产生的热量________(填“增大”、“减小”或“不变)。
③增大的值,则生成乙醇的物质的量____(填“增大”、“减小”、“不变”或“不能确定”)。
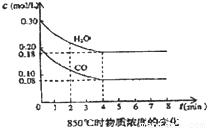
在一体积为10L的容器中,通入一定量的CO和H2O,在85℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-Q kJ/mol CO和H2O浓度变化如图,则
(1)0-4min的平均反应速率v(CO)= mol/
(2)下列能说明反应达到平衡状态的是 .
a、每消耗1mol CO2的同时生成l molH2O b、体系压强保持不变
c、v正(CO)=v逆(CO2) d、容器中混合气体的密度保持不变
e、混合气体中H2O的体积分数保持不变 f、CO2和H2的体积比保持不变
t1℃时物质浓度(mol/L)的变化
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min-4min之间反应处于 状态;C1数值 0.08mol/L(填大于、小于或等于).
②反应在4min-5min之间,平衡向逆方向移动,可能的原因是 (单选),表中5min-6min之间数值发生变化,可能的原因是 (单选).
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)0-4min的平均反应速率v(CO)= mol/
(2)下列能说明反应达到平衡状态的是 .
a、每消耗1mol CO2的同时生成l molH2O b、体系压强保持不变
c、v正(CO)=v逆(CO2) d、容器中混合气体的密度保持不变
e、混合气体中H2O的体积分数保持不变 f、CO2和H2的体积比保持不变
t1℃时物质浓度(mol/L)的变化
| 时间 | CO | H2O | CO2 | H2 |
| 0.200 | 0.300 | |||
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3min-4min之间反应处于 状态;C1数值 0.08mol/L(填大于、小于或等于).
②反应在4min-5min之间,平衡向逆方向移动,可能的原因是 (单选),表中5min-6min之间数值发生变化,可能的原因是 (单选).
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.
 查看习题详情和答案>>
查看习题详情和答案>>
如何降低大气中CO2的含量及有效地开发利用CO2,已受到各国的普遍重视.
(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从反应开始到平衡,氢气的平均反应速率v(H2)= mol/.
②该反应的平衡常数表达式为 .
③其它条件不变,下列措施中能使
n(CH3OH)/n(CO2)增大的是 .
A.升高温度 B.再充入1mol CO2和3mol H2
C.将H2O(g)从体系中分离 D.充入He(g),使体系压强增大
(2)CO2是典型的酸性氧化物,能转化为其它物质.
①利用CO2可制得纯碱,纯碱溶液PH 7(填大于、等于、小于);原因是(用离子反应方程式表示) .
②一定温度下,在碳酸钙饱和溶液中滴加饱和碳酸钠溶液,观察到的现象是 ;产生此现象的原因是 .
(3)在载人航天器的生态系统中,不仅要求分离除去CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2 ,CO可用作燃料.已知该反应的阳极反应为:4OH--4e-=O2↑+2H2O则阴极反应式为: .
 查看习题详情和答案>>
查看习题详情和答案>>
(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从反应开始到平衡,氢气的平均反应速率v(H2)= mol/.
②该反应的平衡常数表达式为 .
③其它条件不变,下列措施中能使
n(CH3OH)/n(CO2)增大的是 .
A.升高温度 B.再充入1mol CO2和3mol H2
C.将H2O(g)从体系中分离 D.充入He(g),使体系压强增大
(2)CO2是典型的酸性氧化物,能转化为其它物质.
①利用CO2可制得纯碱,纯碱溶液PH 7(填大于、等于、小于);原因是(用离子反应方程式表示) .
②一定温度下,在碳酸钙饱和溶液中滴加饱和碳酸钠溶液,观察到的现象是 ;产生此现象的原因是 .
(3)在载人航天器的生态系统中,不仅要求分离除去CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2 ,CO可用作燃料.已知该反应的阳极反应为:4OH--4e-=O2↑+2H2O则阴极反应式为: .
 查看习题详情和答案>>
查看习题详情和答案>>