摘要:10.研析:由质量守恒定律得.反应所生成的氢气为:20g+50g -69.8g =0.2g (1)设此黄铜中锌的质量为x.反应消耗H2SO4的质量为y.生成ZnSO4的质量为z Zn +H2SO4=ZnSO4+H2↑ 65 98 161 2 x y z 0.2g 65g/x=2g/0.2g,98g/y=2g/0.2g,161g/z=2g/0.2g 解得:x=6.5g y=9.8g z=16.1g 此黄铜样品中铜的质量为:20g -6.5g =13.5g 此黄铜样品中铜的质量分数为: 13.5g÷20g×100%=67.5% (2)反应后溶液的质量是:69.8g -13.5g =56.3g 所得溶液的溶质质量分数为:16.1g÷56.3g×100%=28.6% 答案:此黄铜中铜的质量分数是67.5%.所得溶液的溶质质量分数是28.6%
网址:http://m.1010jiajiao.com/timu3_id_322098[举报]
同温同压下,1体积氮气和3体积氢气化合生成2体积氨气,已知氮气和氢气都由简单分子构成,推断他们都是双原子分子和氨的化学式的主要依据是①阿伏加德罗定律 ②质量守恒定律③原子或分子数只能为整数 ④化合价规则( )
查看习题详情和答案>>
同温同压下,1体积氮气和3体积氢气化合生成2体积氨气。已知氮气和氢气都由最简单分子构成,推断它们都是双原子分子和氨的化学式的主要依据是( )
①阿伏加德罗定律 ②质量守恒定律 ③原子或分子数只能为整数 ④化合价规则
A.①③ B.①②③ C.①②④ D.①②③④
查看习题详情和答案>>
同温同压下,1体积氮气和3体积氢气化合生成2体积氨气。已知氮气和氢气都由最简单分子构成,推断他们都是双原子分子和氨的化学式的主要依据是( )
①阿伏加德罗定律 ②质量守恒定律 ③原子或分子数只能为整数 ④化合价规则
A.①③ B.①②③ C.①②④ D.①②③④
查看习题详情和答案>>(8分)现有①KMnO4 ②H2 ③O2 ④CL2 ⑤CO ⑥AL 六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲:_____ 中,常用的还原剂放入乙:_____中,则:
⑴甲中有 ;乙中有 。(填序号)
⑵由Fe  Fe3O4
,Fe2O3
Fe3O4
,Fe2O3
 Fe 可知,欲实现I反应过程应从___________
(填“甲”或“乙”,下同)中找物质,欲实现II反应过程应从 中找物质。
Fe 可知,欲实现I反应过程应从___________
(填“甲”或“乙”,下同)中找物质,欲实现II反应过程应从 中找物质。
⑶请将4种物质:Fe、Fe2O3、CO、CO2分别填入下面对应的横线上,组成一个配平了的化学方程式,并标出电子转移的方向和数目。(提示:反应物是Fe2O3和3 CO )

 +
=====
+
+
=====
+
⑷一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为:
4X+5O2 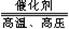 4NO+6H2O,则根据质量守恒定律可以推出X的化学式为
。
4NO+6H2O,则根据质量守恒定律可以推出X的化学式为
。
查看习题详情和答案>>