摘要:36.某常见金属A及其化合物B.C之间有如下的转化关系: ①写出A.C的化学式:A .C . ②写出B→C的离子方程式 .
网址:http://m.1010jiajiao.com/timu3_id_319546[举报]
 某常见金属A及其化合物之间有如下的转化关系:
某常见金属A及其化合物之间有如下的转化关系:①写出A、C的化学式:A
Fe
Fe
,CFeCl2
FeCl2
.②写出B→C的离子方程式
2Fe3++Fe═3Fe2+
2Fe3++Fe═3Fe2+
.A、B、C、D、E、F、G、H、I、J都是中学化学中的常见物质,各物质之间的转化关系如下图所示

已知:
①图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素。
②D为地壳中含量最高的元素组成的单质;E为酸性氧化物,不溶于水,能与某种酸反应;F不溶于水;H为淡黄色固体化合物;C为离子化合物,阴、阳离子均含有金属元素。
③电解饱和J溶液是工业上的重要反应。
(1)A、B、C中共同含有的第三周期元素是________________。
(2)H的电子式是__________。
(3)E→G的离子方程式是__________________。
(4)常温下测得一定浓度的C溶液的pH=10,用离子方程式表示其原因:__________________。向C溶液中通入过量CO2的离子方程式为_________________________。
(5)按物质的性质分类,上述物质中涉及_______种氧化物。
查看习题详情和答案>>
①图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素。
②D为地壳中含量最高的元素组成的单质;E为酸性氧化物,不溶于水,能与某种酸反应;F不溶于水;H为淡黄色固体化合物;C为离子化合物,阴、阳离子均含有金属元素。
③电解饱和J溶液是工业上的重要反应。
(1)A、B、C中共同含有的第三周期元素是________________。
(2)H的电子式是__________。
(3)E→G的离子方程式是__________________。
(4)常温下测得一定浓度的C溶液的pH=10,用离子方程式表示其原因:__________________。向C溶液中通入过量CO2的离子方程式为_________________________。
(5)按物质的性质分类,上述物质中涉及_______种氧化物。
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含一种金属元素。A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物甲和乙(相对分子质量甲<乙)。
请回答下列问题:
(1)写出乙的一种用途______________。
(2)用某种废弃的金属易拉罐与A、C、D组成的化合物溶液反应,所产生的气体可充填气球,请写出该反应的离子方程式___________,使用这种气球存在的隐患是_____________。
(3)已知A、B、C三种元素组成的某盐溶液常温下呈酸性,请用离子方程式表示其原因:__________。向0.02 mol·L-1的CuSO4溶液中加入由A、D、C三种元素组成的溶液来调节pH时,应使溶液的pH大于__________才能生成Cu(OH)2沉淀。[己知常温下Cu((OH)2(s) Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
(4) 在一定温度下,向一个体积为2L的密闭容器中,通入3 mol EC2和2 mol C2及固体催化剂,使之反应:2 EC2(g) + C2 (g) 2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
①加入3 mol EC2和2 mol C2发生反应,达到平衡时放出的热量为___________________。
②该温度下反应的平衡常数是________________。
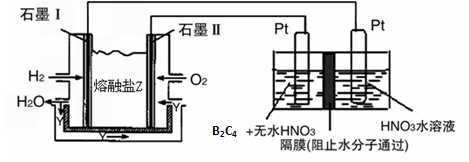
(5) B2C5是一种新型硝化剂,其性质和制备受到人们的关注。现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备B2C5,装置如下图所示,其中Y为CO2。写出石墨I 电极上发生反应的电极反应式 ______________。
(1)写出乙的一种用途______________。
(2)用某种废弃的金属易拉罐与A、C、D组成的化合物溶液反应,所产生的气体可充填气球,请写出该反应的离子方程式___________,使用这种气球存在的隐患是_____________。
(3)已知A、B、C三种元素组成的某盐溶液常温下呈酸性,请用离子方程式表示其原因:__________。向0.02 mol·L-1的CuSO4溶液中加入由A、D、C三种元素组成的溶液来调节pH时,应使溶液的pH大于__________才能生成Cu(OH)2沉淀。[己知常温下Cu((OH)2(s)
 Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
Cu2+(aq)+2OH-(aq), Ksp=2×10-20] (4) 在一定温度下,向一个体积为2L的密闭容器中,通入3 mol EC2和2 mol C2及固体催化剂,使之反应:2 EC2(g) + C2 (g)
 2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。①加入3 mol EC2和2 mol C2发生反应,达到平衡时放出的热量为___________________。
②该温度下反应的平衡常数是________________。
(5) B2C5是一种新型硝化剂,其性质和制备受到人们的关注。现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备B2C5,装置如下图所示,其中Y为CO2。写出石墨I 电极上发生反应的电极反应式 ______________。
A、B、C均为中学化学常见的单质,其中一种是金属,通常状况下,A为固体,B为黄绿色气体,C为气体,其余均为化合物,X是一种常用的具有挥发性的无氧强酸,E为黑色固体,H为无色液体,它们之间的转化关系如图(其中某些反应条件和产物已略去)。
 |
(1)写出:A的化学式 ,F的化学式 。
(2)在反应①~⑦中,不属于氧化还原反应的是 (填序号)。
(3)完成:E和X反应的离子方程式: ;
(4)完成H和某种化合物快速制C的化学方程式 ,每生成0.15molC电子转移 mol。
(5)B蒸气与过量氨气混合有白烟及另一种气体单质产生,该反应的化学方程式为:
。
查看习题详情和答案>>