摘要:按图所表示的装置进行实验: (1)实验开始一段时间后.可观察到锥形瓶口上方有白烟生成.请将可能观察到的其他现象补齐 .有关化学方程式为 . (2)由于气温的原因.上述实验一段时间后现象不太明显.应该向锥形瓶内加入下列哪种物质才能看到明显的现象 . A.NaOH固体或生石灰 B.浓H2SO4 C.NH4Cl固体 (3)经过对比试验证明.在其他条件相同时.用空气代替氧气的实验效果较差.主要原因是 .
网址:http://m.1010jiajiao.com/timu3_id_318527[举报]
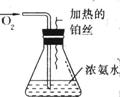 按图所表示的装置进行实验:
按图所表示的装置进行实验:
(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到的其他现象补齐_________.有关化学方程式为________________
(2)由于气温的原因,上述实验一段时间后现象不太明显,应该向锥形瓶内加入下列哪种物质才能看到明显的现象________(填字母)。
A.NaOH固体 B.生石灰 C.浓H2SO4 D.NH4Cl固体
(3)经过对比试验证明。在其他条件相同时,用空气代替氧气的实验效果较差,主要原因是 __________________
查看习题详情和答案>>(7分)按图所表示的装置进行实验:
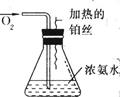
(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到的其他现象补齐_________.有关化学方程式为________________
(2)由于气温的原因,上述实验一段时间后现象不太明显,应该向锥形瓶内加入下列哪种物质才能看到明显的现象________(填字母)。
(3)经过对比试验证明。在其他条件相同时,用空气代替氧气的实验效果较差,主要原因是 __________________

(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到的其他现象补齐_________.有关化学方程式为________________
(2)由于气温的原因,上述实验一段时间后现象不太明显,应该向锥形瓶内加入下列哪种物质才能看到明显的现象________(填字母)。
| A.NaOH固体 | B.生石灰 | C.浓H2SO4 | D.NH4Cl固体 |
按下图所表示的装置、方法进行实验:

(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到其他现象补齐:_______________________。有关化学方程式为_______________________。
(2)由于气温的原因,上述实验一段时间后现象不太明显,需向锥形瓶内加入下列哪种物质才能重新看到明显的现象(填代号)_____。
A.NaOH B. CaO C. 浓H2SO4 D. NH4Cl
(3)经过对比实验证明,在其他条件相同时,用空气代替氧气的实验效果较差,主要原因是_______________________________。
查看习题详情和答案>>某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置: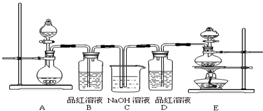
(1)实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为:
B
(3)装置C的作用是
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验: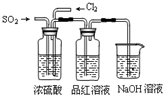
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅,试根据该实验装置和两名同学的实验结果
①指出在气体进入品红溶液之前,先将SO2和Cl2通过浓硫酸的两个目的
②试分析甲同学实验过程中,品红溶液不褪色的原因是:
③你认为乙同学是怎样做到让品红溶液变得越来越浅的?
查看习题详情和答案>>

(1)实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质
酸性
酸性
,还原性
还原性
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为:
B
溶液由无色变成红色
溶液由无色变成红色
D溶液没有明显变化
溶液没有明显变化
(3)装置C的作用是
吸收多余的SO2和Cl2,防止污染环境
吸收多余的SO2和Cl2,防止污染环境
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验:

通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅,试根据该实验装置和两名同学的实验结果
①指出在气体进入品红溶液之前,先将SO2和Cl2通过浓硫酸的两个目的
使SO2和Cl2混合均匀,
使SO2和Cl2混合均匀,
、通过观察气泡控制气体的流速
通过观察气泡控制气体的流速
.②试分析甲同学实验过程中,品红溶液不褪色的原因是:
控制SO2和Cl2按物质的量之比1:1进气,二者发生反应,
控制SO2和Cl2按物质的量之比1:1进气,二者发生反应,
、生成无漂白性的H2SO4和HCl
生成无漂白性的H2SO4和HCl
,并用离子方程式表示SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
、SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
③你认为乙同学是怎样做到让品红溶液变得越来越浅的?
控制SO2和Cl2进气的物质的量,使之不相等
控制SO2和Cl2进气的物质的量,使之不相等
.某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置:

(1)实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质______,______
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为:
B______ D______
(3)装置C的作用是______
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验:

通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅,试根据该实验装置和两名同学的实验结果
①指出在气体进入品红溶液之前,先将SO2和Cl2通过浓硫酸的两个目的______、______.
②试分析甲同学实验过程中,品红溶液不褪色的原因是:______、______,并用离子方程式表示______、______
③你认为乙同学是怎样做到让品红溶液变得越来越浅的?______.
查看习题详情和答案>>

(1)实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质______,______
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为:
B______ D______
(3)装置C的作用是______
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验:

通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅,试根据该实验装置和两名同学的实验结果
①指出在气体进入品红溶液之前,先将SO2和Cl2通过浓硫酸的两个目的______、______.
②试分析甲同学实验过程中,品红溶液不褪色的原因是:______、______,并用离子方程式表示______、______
③你认为乙同学是怎样做到让品红溶液变得越来越浅的?______.