摘要:13.关于可逆反应C(s)+ CO2(g) 2C0(g),△H > 0 平衡常数为K.下列说法错误的是 A. k = B. K值越大表示达到平衡时.正反应进行程度越大 C.其它条件不变时.温度改变.K值改变 D.其它条件不变时.压强改变.K值不改变
网址:http://m.1010jiajiao.com/timu3_id_318025[举报]
关于可逆反应A(s)+B(g)?2C(g);△H<0,平衡常数为K,下列说法正确的是( )
A、K=
| ||
| B、K值越大表示达到平衡时,正反应进行程度越大 | ||
| C、其它条件不变时,温度升高,K值增大 | ||
| D、其它条件不变时,压强减小,K值减小 |
|
工业上由粗硅制纯硅采取如下方法: Si(s)+3HCl(g) SiHCl3+H2(g) 下列关于上述反应的说法中正确的是 | |
A. |
反应①、②均为置换反应和氧化还原反应 |
B. |
反应①、②实际为可逆反应 |
C. |
由于反应①放热,则反应②一定吸热 |
D. |
不能确定反应②为吸热或放热 |
 I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,X和Y两物质的浓度随时间变化情况如图.
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):
Y 2X
2X
 2X
2XY 2X
2X
. 2X
2X(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是
b、d
b、d
.II.如图是可逆反应X2+3Y2
 2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是B、D
B、D
.
A、t1时,只有正方向反应
B、t2时,反应到达限度
C、t2-t3,反应不再发生
D、t2-t3,各物质的浓度不再发生变化
III.以下是关于化学反应2SO2+O2
 2SO3 的两个素材:
2SO3 的两个素材:素材1:某温度和压强下,2升容器中,不同时间点测得密闭体系中三种物质的物质的量

素材2:在不同条件下进行时测得SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数)

从以上的两个素材中体会:
(1)根据素材1中计算20-30s期间,用二氧化硫表示的化学反应的平均速率为:
0.0075mol?L-1?s-1
0.0075mol?L-1?s-1
.(2)根据素材2中分析得到,提高该化学反应限度的途径有:
增大压强或在一定范围内降低温度
增大压强或在一定范围内降低温度
.(3)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应条件是
温度为600℃,压强为1MPa
温度为600℃,压强为1MPa
.关于下列图示的说法中正确的是( )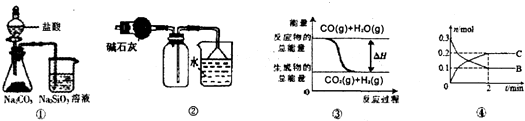

| A、由图①所示实验可得出三种元素的非金属性强弱顺序是:氯>碳>硅 | B、图②可用于干燥、收集氯化氢,并吸收多余的氯化氢 | C、图③表示可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 | D、对反应:A(s)+2B(g)?xC(g),根据图④可以求出x=2 |
下列关于反应过程中能量变化的说法正确的是( )


| A、在一定条件下,某可逆反应的△H=+100kJ?mol-1,则该反应正反应活化能比逆反应活化能大100kJ?mol-1 | B、图中A、B曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0未使用和使用催化剂时,反应过程中的能量变化 | C、同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | D、己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2.则△H1>△H2 |