摘要: 正极 (2)Zn与Cu2+反应生成Cu.Zn与Cu构成原电池.加快反应速率 (3)2H++2e-=H2↑(写2H2O+2e- = H2↑+2OH-不得分.因为“酸化 ) 87g
网址:http://m.1010jiajiao.com/timu3_id_317745[举报]
(2009?山东)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
(1)该电池的负极材料是
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀.其主要原因是
a.NaOH b.Zn c.Fe d.NH3?H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是:
查看习题详情和答案>>
(1)该电池的负极材料是
Zn
Zn
.电池工作时,电子流向正极
正极
(填“正极”或“负极”).(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀.其主要原因是
锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀
锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀
.欲除去Cu2+,最好选用下列试剂中的b
b
(填代号).a.NaOH b.Zn c.Fe d.NH3?H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是:
2H++2e-=H2↑
2H++2e-=H2↑
.若电解电路中通过2mol电子,MnO2的理论产量为87g
87g
.将锌片和铜片插入某种电解质溶液中,如图所示装置.
(1)若电解质溶液是稀硫酸①锌片与铜片不用导线连接,现象是
反应的离子方程式
②若用导线把金属片连接起来,现象是
则发生氧化反应的是
(2)若电解质溶液是硫酸铜溶液,用导线把金属片连接起来在导线中电子是由
查看习题详情和答案>>
(1)若电解质溶液是稀硫酸①锌片与铜片不用导线连接,现象是
锌片上有气泡产生,铜片上无现象
锌片上有气泡产生,铜片上无现象
,反应的离子方程式
Zn+2H+=Zn2++H2↑
Zn+2H+=Zn2++H2↑
.②若用导线把金属片连接起来,现象是
锌片逐渐溶解,铜片上有气泡生成
锌片逐渐溶解,铜片上有气泡生成
,则发生氧化反应的是
锌
锌
极(填“锌”或“铜”)铜极发生的反应是2H++2e-H2↑
2H++2e-H2↑
,该电池的总反应方程式是Zn+2H+=Zn2++H2↑
Zn+2H+=Zn2++H2↑
(2)若电解质溶液是硫酸铜溶液,用导线把金属片连接起来在导线中电子是由
锌
锌
极流向铜
铜
极,电极反应式为负极Zn-2e-=Zn2+
Zn-2e-=Zn2+
Zn-2e-=Zn2+
Zn-2e-=Zn2+
,正极Cu2++2e-Cu
Cu2++2e-Cu
,反应的化学方程式为Zn+CuSO4=ZnSO4+Cu
Zn+CuSO4=ZnSO4+Cu
.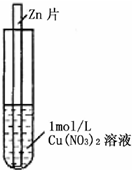 (2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.
(2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.回答下列问题:
(1)反应结束时,试管底部存在的一些蓝色沉淀是什么物质
氢氧化铜
氢氧化铜
,白色沉淀可能是什么物质氢氧化锌
氢氧化锌
,用离子方程式表示实验中观察到的红色固体产生的原因Zn+Cu2+=Cu+Zn2+
Zn+Cu2+=Cu+Zn2+
.(2)有学生甲认为,反应中产生的大量气泡可能是氢气,支持这种说法的理由是
Cu2+水解溶液显酸性,锌在酸性溶液中反应置换出氢气
Cu2+水解溶液显酸性,锌在酸性溶液中反应置换出氢气
.(3)学生乙将反应过程中产生的气体用排水法收集起来,这是一种无色气体,用爆鸣法测试不能产生爆呜声,则学生甲的假设被推翻.学生乙又对这种无色气体进行推测,并设计了一个简便的实验方法证实了他的推测,写出学生乙推测出的这种气体的分子式
NO
NO
;验证该气体的实验方法是在收集到的无色气体中通入空气可变红棕色
在收集到的无色气体中通入空气可变红棕色
.(4)学生丙解释反应速率逐渐加快的原因时,认为除温度升高外还有一个重要因素,请问是什么因素?
锌片表面附着铜,形成铜锌原电池,可加快反应速率
锌片表面附着铜,形成铜锌原电池,可加快反应速率
.(5)起初实验小组同学认为,溶液显绿色可能是Zn(NO3)2溶液的颜色,但学生丁将Zn(NO3)2固体溶于水后却得到无色溶液,他马上回想起该溶液的颜色与浓硝酸和铜片反应后的溶液颜色极为相似,于是他又提出了关于溶液呈绿色的一种新的假设:可能是硝酸铜溶液中溶入了一种气体,这种气体可能是
NO2
NO2
,请设计一个简单的实验验证这种假设正确与否将绿色的混合溶液加热若能放出红棕色气体、且溶液变蓝色,说明这个假设正确或将NO2气体通入蓝色硝酸铜溶液中观察溶液颜色是否变绿色
将绿色的混合溶液加热若能放出红棕色气体、且溶液变蓝色,说明这个假设正确或将NO2气体通入蓝色硝酸铜溶液中观察溶液颜色是否变绿色
.