网址:http://m.1010jiajiao.com/timu3_id_316046[举报]
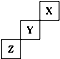 X、Y、Z为三种短周期元素,他们在周期表中的位置关系如图所示.据此回答下列问题:
X、Y、Z为三种短周期元素,他们在周期表中的位置关系如图所示.据此回答下列问题:(1)X元素的名称为
(2)Y元素形成单质的电子式是
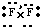
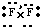
(3)元素Z在自然界中的存在形态为
(4)Y元素、Z元素与H2化合时的能量变化是
(分)X、Y、Z为三种短周期元素,他们在周期表中的位置关系如图所示 。据此回答下列问题:
。据此回答下列问题:
(1)X元素的名称为 ,它形成的单质为 (用分子式表示); He 。若该元素的某种原子内核内中子数与质子数相等,则该原子的摩尔质量是 ;结合最近卫星发回的图片预测,月球的土壤中吸附着数百万吨的![]() ,上述原子与
,上述原子与![]() 的关系是 。
的关系是 。
(2)Y元素形成单质的电子式是 ,Y单质的氧化性 (填“强于”或者“弱于”)O2的氧化性,并用相应的化学方程式说明 。
(3)元素Z在自然界中的存在形态为 (填序号)①只有化合态,②只有游离态,③既有游离态,又有化合态;含Z元素的某些化合物燃烧后会造成严重的大气污染,其主要原因是 。
(4)Y元素、Z元素与H2化合时的能量变化是 ,(填“都放热”、“都吸热”、“前者放热,后者吸热”或者“前者吸热,后者放热”),能量变化的大小关系为前者 (填“>”、“=”或者“<”)。
查看习题详情和答案>>X、Y、Z为三种短周期元素,他们在周期表中的位置关系如图所示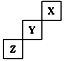 。据此回答下列问题:
。据此回答下列问题:
(1)X元素的名称为 ,它形成的单质为 (用分子式表示); He 。若该元素的某种原子内核内中子数与质子数相等,则该原子的摩尔质量是 ;结合最近卫星发回的图片预测,月球的土壤中吸附着数百万吨的![]() ,上述原子与
,上述原子与![]() 的关系是 。
的关系是 。
(2)Y元素形成单质的电子式是 ,Y单质的氧化性 (填“强于”或者“弱于”)O2的氧化性,并用相应的化学方程式说明 。
(3)元素Z在自然界中的存在形态为 (填序号)①只有化合态,②只有游离态,③既有游离态,又有化合态;含Z元素的某些化合物燃烧后会造成严重的大气污染,其主要原因是 。
(4)Y元素、Z元素与H2化合时的能量变化是 ,(填“都放热”、“都吸热”、“前者放热,后者吸热”或者“前者吸热,后者放热”),能量变化的大小关系为前者 (填“>”、“=”或者“<”)。
查看习题详情和答案>>(1)X元素的名称为______,它形成的单质为______(用分子式表示).若该元素的某种原子内核内中子数与质子数相等,则该原子的摩尔质量是______;结合最近卫星发回的图片预测,月球的土壤中吸附着数百万吨的23He,上述原子与23He的关系是______.
(2)Y元素形成单质的电子式是______,Y单质的氧化性______(填“强于”或者“弱于”)O2的氧化性,并用相应的化学方程式说明______.
(3)元素Z在自然界中的存在形态为______(填序号)①只有化合态,②只有游离态,③既有游离态,又有化合态;含Z元素的某些化合物燃烧后会造成严重的大气污染,其主要原因是______.
(4)Y元素、Z元素与H2化合时的能量变化是______,(填“都放热”、“都吸热”、“前者放热,后者吸热”或者“前者吸热,后者放热”),能量变化的大小关系为前者______(填“>”、“=”或者“<”).

(1)X元素的名称为______,它形成的单质为______(用分子式表示).若该元素的某种原子内核内中子数与质子数相等,则该原子的摩尔质量是______;结合最近卫星发回的图片预测,月球的土壤中吸附着数百万吨的23He,上述原子与23He的关系是______.
(2)Y元素形成单质的电子式是______,Y单质的氧化性______(填“强于”或者“弱于”)O2的氧化性,并用相应的化学方程式说明______.
(3)元素Z在自然界中的存在形态为______(填序号)①只有化合态,②只有游离态,③既有游离态,又有化合态;含Z元素的某些化合物燃烧后会造成严重的大气污染,其主要原因是______.
(4)Y元素、Z元素与H2化合时的能量变化是______,(填“都放热”、“都吸热”、“前者放热,后者吸热”或者“前者吸热,后者放热”),能量变化的大小关系为前者______(填“>”、“=”或者“<”).
 查看习题详情和答案>>
查看习题详情和答案>>