网址:http://m.1010jiajiao.com/timu3_id_315822[举报]
 运用化学反应原理研究元素及其化合物的反应对生产、生活有重要意义.
运用化学反应原理研究元素及其化合物的反应对生产、生活有重要意义.请回答下列问题:
(1)工业上以辉铜矿(主要成分 Cu2S)为原料,采取火法熔炼工艺生产铜.该过程中有如下反应:
2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g)△H=-768.2KJ?mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0KJ?mol-1
则反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的△H=
(2)硫酸生产中涉及反应:2SO2(g)+O2(g)?2SO3(g).
①一定条件下,的平衡转化率和温度的关系如右图所示.该反应的△H
②某温度时,将4molSO2和2molO2通入2L密闭容器中,10min时反应达到平衡状态,测得SO3的浓度为1.6mol?L-1,则0~10min内的平均反应速率v(SO2)=
③下列叙述能证明该反应已经达到化学平衡状态的是(填标号,下同)
A.容器内压强不再发生变化 B.SO2的体积分数不再发生变化?
C.容器内气体质量不再发生变化 D.容器内气体密度不再发生变化?
④以下操作将引起平衡向正反应方向移动并能提高SO2转化率的是
A.向容器中通入少量O2 B.向容器中通入少量SO2?C.使用催化剂 D.升高温度?E.恒容通入少量氦气?
⑤气体SO2是大气污染物,可选用下列试剂中的
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨.
请回答下列问题:
(1)工业上以辉铜矿(主要成分 Cu2S)为原料,采取火法熔炼工艺生产铜.该过程中有如下反应:
2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g)△H=-768.2KJ?mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0KJ?mol-1
则反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的△H=______.
(2)硫酸生产中涉及反应:2SO2(g)+O2(g)?2SO3(g).
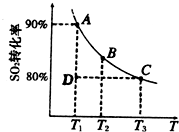
①一定条件下,的平衡转化率和温度的关系如右图所示.该反应的△H______O(填“>”或“<”).反应进行到状态D时,v正______v逆(填“>”、“<”或“=”).?
②某温度时,将4molSO2和2molO2通入2L密闭容器中,10min时反应达到平衡状态,测得SO3的浓度为1.6mol?L-1,则0~10min内的平均反应速率v(SO2)=______,该温度下反应的平衡常数K=______.
③下列叙述能证明该反应已经达到化学平衡状态的是(填标号,下同)______
A.容器内压强不再发生变化 B.SO2的体积分数不再发生变化?
C.容器内气体质量不再发生变化 D.容器内气体密度不再发生变化?
④以下操作将引起平衡向正反应方向移动并能提高SO2转化率的是______?
A.向容器中通入少量O2 B.向容器中通入少量SO2?C.使用催化剂 D.升高温度?E.恒容通入少量氦气?
⑤气体SO2是大气污染物,可选用下列试剂中的______吸收.
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨.
请回答下列问题:
(1)工业上以辉铜矿(主要成分 Cu2S)为原料,采取火法熔炼工艺生产铜.该过程中有如下反应:
2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g)△H=-768.2KJ?mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0KJ?mol-1
则反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的△H= .
(2)硫酸生产中涉及反应:2SO2(g)+O2(g)?2SO3(g).
①一定条件下,的平衡转化率和温度的关系如右图所示.该反应的△H O(填“>”或“<”).反应进行到状态D时,v正 v逆(填“>”、“<”或“=”).?
②某温度时,将4molSO2和2molO2通入2L密闭容器中,10min时反应达到平衡状态,测得SO3的浓度为1.6mol?L-1,则0~10min内的平均反应速率v(SO2)= ,该温度下反应的平衡常数K= .
③下列叙述能证明该反应已经达到化学平衡状态的是(填标号,下同)
A.容器内压强不再发生变化 B.SO2的体积分数不再发生变化?
C.容器内气体质量不再发生变化 D.容器内气体密度不再发生变化?
④以下操作将引起平衡向正反应方向移动并能提高SO2转化率的是 ?
A.向容器中通入少量O2 B.向容器中通入少量SO2?C.使用催化剂 D.升高温度?E.恒容通入少量氦气?
⑤气体SO2是大气污染物,可选用下列试剂中的 吸收.
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨.
 查看习题详情和答案>>
查看习题详情和答案>>
运用化学反应原理研究元素及其化合物的反应对生产、生活有重要意义。
请回答下列问题:
(1)工业上以辉铜矿(主要成分 Cu2S)为原料,采取火法熔炼工艺生产铜。该过程中有如下反应:
2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g) △H=-768.2KJ·mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) △H=+116.0KJ·mol-1
则反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的 △H= 。
 (2)硫酸生产中涉及反应:2SO
(2)硫酸生产中涉及反应:2SO![]() (g)+O
(g)+O![]() (g)
(g)![]() 2SO
2SO![]() (g)。 ① 一定条件下,的平衡转化率和温度的关系如右图所示。该反应的ΔH O(填“>”或“<”)。反应进行到状态D时,v正 v逆(填“>”、“<”或“=”)。
(g)。 ① 一定条件下,的平衡转化率和温度的关系如右图所示。该反应的ΔH O(填“>”或“<”)。反应进行到状态D时,v正 v逆(填“>”、“<”或“=”)。
② 某温度时,将4molSO2和2molO2通入2L密闭容器中,10min时反应达到平衡状态,测得SO3的浓度为1.6mol·L-1,则0~10min内的平均反应速率v(SO2)= ,该温度下反应的平衡常数K= 。
③ 下列叙述能证明该反应已经达到化学平衡状态的是(填标号,下同)
A.容器内压强不再发生变化 B.SO![]() 的体积分数不再发生变化
的体积分数不再发生变化
C.容器内气体质量不再发生变化 D.容器内气体密度不再发生变化
④ 以下操作将引起平衡向正反应方向移动并能提高SO![]() 转化率的是
转化率的是
A.向容器中通入少量O![]() B.向容器中通入少量SO
B.向容器中通入少量SO![]()
C.使用催化剂 D.升高温度 E.恒容通入少量氦气
⑤ 气体SO2是大气污染物,可选用下列试剂中的_______吸收。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨
查看习题详情和答案>>2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g)△H=-768.2KJ?mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0KJ?mol-1
反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的△H=
在上述工业生产过程中产生的SO2气体直接排放会污染大气.工业上常用氨水吸收SO2,反应的化学方程式为
Ⅱ大气污染的另一个重要问题是臭氧层的破坏.为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4(g)+H2(g)
| 催化剂 |
| △ |
如果不考虑反应过程中的副反应,在一个密闭容器中发生上述反应,该反应达到平衡后,测得下表中的数据.
| 实验序号 | 温度℃ | 初始CCl4浓度(mol?L-1) | 初始H2浓度(mol?L-1) | CCl4的转化率 |
| 1 | 110 | 0.8 | 1.2 | a |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 120 | 1 | 2 | x |
| 4 | 120 | 1 | 4 |
(1)实验1中,CCl4的转化率a
(2)在实验2的平衡体系中,再加入0.5mol?L-1CCl4和1mol?L-1HCl,平衡将向
(3)120℃,在相同条件的密闭容器中,分别进行实验3、4,测得CCl4的转化率(x)和生成物中CHCl3的体积分数(y)随时间(t)的变化关系如图(图中实线是CCl4转化率变化曲线,虚线是产物中CHCl3的体积分数变化曲线).
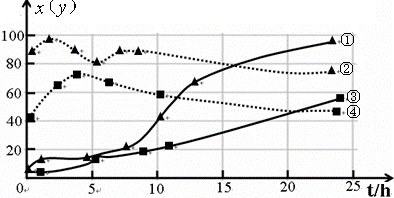
图中的四条线中,表示H2起始浓度为2mol?L-1实验中CCl4的转化率(x)变化曲线是