网址:http://m.1010jiajiao.com/timu3_id_315514[举报]
| 污染指数 | 首要污染物 | 空气质量等级 | 空气质量状况 |
| 55 | SO2 | Ⅱ | 良 |
(1)用如图所示装置进行实验.

①A装置的作用是
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变
③D装置的作用是
(2)往盛有水的烧杯中通入SO2气体,测得所得溶液的pH
(3)SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,则在此过程中的飘尘是作为
(4)SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为
(10分)酸雨是指pH<5.6的雨、雪等各种形式的大气降水。二氧化硫是形成酸雨的主要因素之一,它主要是由含硫燃料(煤和石油)燃烧和金属冶炼厂释放的二氧化硫气体造成。酸雨的危害极大,减少二氧化硫等污染物的排放,保护环境是非常重要的。某校化学兴趣小组的学生,分成两组对酸雨及空气中二氧化硫的含量进行了测定。
第一组,取刚降到地面的酸雨水样,进行了如下实验:
(1)将一片红色的玫瑰花瓣浸在一份水样中
(2)向雨水试样中滴加氯化钡溶液,有白色浑浊出现
(3)每隔一定时间测定其pH,数据如表Ⅰ所示。
表Ⅰ 不同时间酸雨的pH
| 测定时间/小时钟 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(1)一段时间后,观察到红色变浅,可能的原因是 ▲
(2)生成白色浑浊的离子方程式 ▲
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示) ▲
(4)如果取该雨水和蒸馏水混合,再测pH,结果将 ▲ (填“变大”“变小”或“不变”)
第二组,用拟用下列装置定量分析空气中SO2的含量:

(5)该组同学查资料得到的反应原理为:SO2与酸性KMnO4溶液反应的离子方程式
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+。
该反应的现象是 ▲ ,SO2在该反应中显 ▲ (填“氧化”或“还原”)性。发生了 ▲ 反应(填“氧化”或“还原”)
(6)通入空气前应进行的实验操作是 ▲ ;KMnO4溶液中导管末端做成球状多孔结构的作用是 ▲
(7)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为 ▲ g/L
查看习题详情和答案>>国家环保总局“环境监测公报”中指出,减少SO2等有害气体的排放和生活废水的处理是我国“十一五”期间环境保护的主要任务.保护我们赖以生存的环境应该成为我们每个人的自觉行动.下面是一些有关大气污染及治理的问题,请回答相关的内容:
(1)分析某地几年内的降雨成分发现,前些年雨水中阴离子主要以SO2-4离子为主,近几年雨水中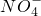 离子的比例有呈明显上升的趋势.通过该地的雨水样本分析,推测该地的大气污染特征是______.
离子的比例有呈明显上升的趋势.通过该地的雨水样本分析,推测该地的大气污染特征是______.
A.煤烟型
B.机动车尾气型
C.由煤烟型向煤烟型与机动车尾气混合型转化
D.由机动车尾气型向煤烟型与机动车尾气混合型转化
(2)某校研究性学习小组收集到一酸雨样本,他们将样本置于敞口容器中并对样本进行一段时间的pH值测定,其测定结果见下表:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 | 6 | 6 |
| 样本的Ph | 4.93 | 4.72 | 4.63 | 4.58 | 4.56 | 4.55 | 4.55 |
(3)在工业上采用氨法烟气脱硫技术.其做法是用氨吸收烟气中的SO2生成亚硫酸铵和亚硫酸氢铵,再用一定量的磷酸进行反应,在反应回收SO2后的混合手中通入适量的氨气得到一种复合肥.氨水吸收SO2生成亚硫酸铵的化学方程式______.
(4)为将SO2的污染变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2和得到单质硫.该方法涉及到的化学反应有:
A.XSO2+2XCO═2xCO2+Sx
B.xCO+Sx═xCOS
C.2XCOS+xSO2═2xCO2+3Sx
其中属于氧化还原反应的是______(填字母).COS分子的电子式为______.
(5)含氮氧化物的气体可以用NH3在一定条件下进行处理,变成两种无毒的物质后排放.下列流程是探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).为比较不同催化剂的催化性能,需要测量并记录的数据是______.在催化剂存在下NH3还原NO的化学方程式______. 查看习题详情和答案>>
(1)分析某地几年内的降雨成分发现,前些年雨水中阴离子主要以SO2-4离子为主,近几年雨水中
| NO | - 4 |
A.煤烟型
B.机动车尾气型
C.由煤烟型向煤烟型与机动车尾气混合型转化
D.由机动车尾气型向煤烟型与机动车尾气混合型转化
(2)某校研究性学习小组收集到一酸雨样本,他们将样本置于敞口容器中并对样本进行一段时间的pH值测定,其测定结果见下表:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 | 6 | 6 |
| 样本的Ph | 4.93 | 4.72 | 4.63 | 4.58 | 4.56 | 4.55 | 4.55 |
(3)在工业上采用氨法烟气脱硫技术.其做法是用氨吸收烟气中的SO2生成亚硫酸铵和亚硫酸氢铵,再用一定量的磷酸进行反应,在反应回收SO2后的混合手中通入适量的氨气得到一种复合肥.氨水吸收SO2生成亚硫酸铵的化学方程式
(4)为将SO2的污染变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2和得到单质硫.该方法涉及到的化学反应有:
A.XSO2+2XCO═2xCO2+Sx
B.xCO+Sx═xCOS
C.2XCOS+xSO2═2xCO2+3Sx
其中属于氧化还原反应的是
(5)含氮氧化物的气体可以用NH3在一定条件下进行处理,变成两种无毒的物质后排放.下列流程是探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).为比较不同催化剂的催化性能,需要测量并记录的数据是
B.火山灰的主要成分为矿物粉尘,其物质组成为硅酸盐与铝酸盐,与形成酸雨的硫、氮氧化物无关
C.火山灰的主要成分为硅酸盐与铝酸盐等弱酸盐,所以能吸收火山喷发的酸性气体形成酸性溶液,从而降低酸雨的危害
D.由于火山喷发所产生的气体中,主要成分为水蒸气、CO、CO2及少量氮与硫的氧化物,所以火山喷发的气体的对环境与人类没有多大影响