网址:http://m.1010jiajiao.com/timu3_id_315372[举报]
在一固定容积的密闭容器中,进行如下反应:
C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
27.反应后物质的总能量增大,则该反应为________反应(填“吸热”或“放热”)。
28.不能判断该反应是否达到化学平衡状态的是________(选填编号)。
a.容器中气体压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(H2O)=c(CO)
29.若容器容积为2L,反应10s后测得混合气体的总质量增加了2.4g, 则CO的平均反应速率为 mol/(L?S);若再增加固态碳的量,则正反应的速率 (选填“增大”、“减小”、“不变”)。
在一固定容积的密闭容器中,进行如下反应:
C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
27.反应后物质的总能量增大,则该反应为________反应(填“吸热”或“放热”)。
28.不能判断该反应是否达到化学平衡状态的是________(选填编号)。
a.容器中气体压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(H2O)=c(CO)
29.若容器容积为2L,反应10s后测得混合气体的总质量增加了2.4g, 则CO的平均反应速率为 mol/(L?S);若再增加固态碳的量,则正反应的速率 (选填“增大”、“减小”、“不变”)。
查看习题详情和答案>>
C(s)+H2O(g)
 CO(g)+H2(g)
CO(g)+H2(g) 27.反应后物质的总能量增大,则该反应为________反应(填“吸热”或“放热”)。
28.不能判断该反应是否达到化学平衡状态的是________(选填编号)。
a.容器中气体压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(H2O)=c(CO)
29.若容器容积为2L,反应10s后测得混合气体的总质量增加了2.4g, 则CO的平均反应速率为 mol/(L?S);若再增加固态碳的量,则正反应的速率 (选填“增大”、“减小”、“不变”)。
(共12分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
Ⅰ.目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25 mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O(g)的浓度随时间变化如下图所示:
(1)从反应开始到平衡,氢气的平均反应速率 = mol/(L·min)
= mol/(L·min)
(2)该条件下CO2的转化率为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
| A.升高温度 | B.恒容时充入氮气 |
| C.将水蒸气从体系中分离 | D.用更有效的催化剂 |

(1)M极的电极材料为 。
(2)加入乙醇的铂电极的电极反应式为 。
(3)在此过程中乙池中某一电极析出金属银4.32g时,此时乙池溶液的体积为400mL,则乙池中溶液的pH为 。
(4)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为 。 查看习题详情和答案>>
(共12分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
Ⅰ.目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25 mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O(g)的浓度随时间变化如下图所示:

(1)从反应开始到平衡,氢气的平均反应速率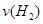 = mol/(L·min)
= mol/(L·min)
(2)该条件下CO2的转化率为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.恒容时充入氮气
C.将水蒸气从体系中分离 D.用更有效的催化剂
Ⅱ.下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:

(1)M极的电极材料为 。
(2)加入乙醇的铂电极的电极反应式为 。
(3)在此过程中乙池中某一电极析出金属银4.32g时,此时乙池溶液的体积为400mL,则乙池中溶液的pH为 。
(4)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为 。
查看习题详情和答案>>