摘要:21.②加催化剂,达到平衡的时间缩短.平衡时A的浓度未变 ③温度升高,达到平衡的时间缩短.平衡时A的浓度减小 ,0.06mol/L, (3)﹥,升高温度向正方向移动.故该反应是吸热反应 -1,0.008mol-1
网址:http://m.1010jiajiao.com/timu3_id_314515[举报]
一定条件下的密闭容器中,进行如反应:NO(g)+CO(g)
N2(g)+CO2(g);△H=-373.2kJ/mol
为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是( )
| 1 |
| 2 |
为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是( )
| A、加(正)催化剂 |
| B、增大压强(体积减小) |
| C、给体系加热 |
| D、从体系中不断移去部分CO2 |
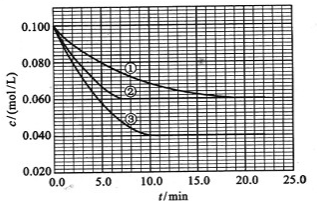 (2013?潍坊模拟)在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.1mol/L,c(B)=0.2mol/L及c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.
(2013?潍坊模拟)在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.1mol/L,c(B)=0.2mol/L及c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由是:
②
加催化剂;达到平衡的时间缩短,平衡时A的浓度未变
加催化剂;达到平衡的时间缩短,平衡时A的浓度未变
;③
温度升高;达到平衡的时间缩短,平衡时A的浓度减小
温度升高;达到平衡的时间缩短,平衡时A的浓度减小
;(2)实验②平衡时B的转化率为
40%(或0.4)
40%(或0.4)
;实验③平衡时C的浓度为0.06mol/L
0.06mol/L
;(3)该反应为
吸热
吸热
(填“吸热”或“放热”)反应,判断其理由是升高温度向正方向移动,故该反应是吸热反应
升高温度向正方向移动,故该反应是吸热反应
;(4)该反应进行到4.0min时的平均反应速度率:
实验②:vB=
0.014mol(L?min)-1
0.014mol(L?min)-1
,实验③:vC=0.008mol(L?min)-1
0.008mol(L?min)-1
. (2010?湖北)在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L 及 c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.
(2010?湖北)在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L 及 c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由是:
②
加催化剂
加催化剂
;达到平衡的时间缩短,平衡时A的浓度未变
达到平衡的时间缩短,平衡时A的浓度未变
.③
温度升高
温度升高
;达到平衡的时间缩短,平衡时A的浓度减小
达到平衡的时间缩短,平衡时A的浓度减小
.(2)实验②平衡时B的转化率为
40%
40%
;实验③平衡时C的浓度为0.06mol/L
0.06mol/L
;(3)该反应的△H
>
>
0,其判断理由是温度升高,平衡向正反应方向移动,
温度升高,平衡向正反应方向移动,
(4)该反应进行到4.0min时的平均反应速率:
实验②:vB=
0.014mol(L?min)-1
0.014mol(L?min)-1
实验③:vc=
0.009mol(L?min)-1
0.009mol(L?min)-1
.对于可逆反应N2(g)+3H2(g)2NH3(g);△H<0,下列研究目的和示意图相符的是
|
| A | B | C | D |
| 研究目的 | 压强对反应的 影响(P2>P1) | 温度对反应的影响 | 增加N2的浓度对反应的影响 | 催化剂对反应的 影响 |
| 图示 | | | | |
【解析】氨气的合成是体积减小的放热的可逆反应,压强越大,反应速率越大,到达平衡的时间就越少,A不正确。升高温度,平衡向逆反应方向移动,所以氮气的转化率降低,B不正确。增大氮气浓度,平衡向向正反应方向移动,C正确。催化剂能加快反应速率,缩短到达平衡的时间,D不正确。答案是C。
查看习题详情和答案>>
对于可逆反应N2(g)+3H2(g) 2NH3(g);△H<0,下列研究目的和示意图相符的是
2NH3(g);△H<0,下列研究目的和示意图相符的是
|
|
A |
B |
C |
D |
|
研究目的 |
压强对反应的 影响(P2>P1) |
温度对反应的影响 |
增加N2的浓度对反应的影响 |
催化剂对反应的 影响 |
|
图示 |
|
|
|
|
【解析】氨气的合成是体积减小的放热的可逆反应,压强越大,反应速率越大,到达平衡的时间就越少,A不正确。升高温度,平衡向逆反应方向移动,所以氮气的转化率降低,B不正确。增大氮气浓度,平衡向向正反应方向移动,C正确。催化剂能加快反应速率,缩短到达平衡的时间,D不正确。答案是C。
查看习题详情和答案>>



