摘要:在一定温度下.容器内某一反应中M.N的物质的量随反应时间变化的曲线如右图.下列表述中正确的是 A.反应的化学方程式为:2MN B.t2时.正.逆反应速率相等.达到平衡 C.t3时.正反应速率大于逆反应速率 D.t1时.N的浓度是M浓度的2倍 20有反应A2+B22AB,在温度和压强可变条件下.产物AB的生成情况如图所示:a为500 ℃.b为300 ℃.从t3开始压缩容器.则下列叙述正确的是 A.AB为气体.A2.B2中必有一种为非气体,正反应吸热 B.AB为气体.A2.B2中必有一种为非气体,正反应放热 C.AB为固体.A2.B2中必有一种为非气体,正反应放热 D.A2.B2.AB均为气体,正反应吸热
网址:http://m.1010jiajiao.com/timu3_id_314486[举报]
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )| A、反应的方程式为M?2N | B、t1时,N的浓度是M浓度的0.5倍 | C、t2时,正逆反应速率相等,达到平衡 | D、t3时,正反应速率大于逆反应速率 |
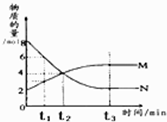 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M | B、t2时,反应不再发生 | C、t2时,正反应速率等于逆反应速率 | D、t3后,反应到达最大限度 |
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )