摘要:下列物质中.能与镁反应产生氢气的是 A.二氧化碳 B.醋酸溶液 C.乙烷 D.碳酸钠溶液
网址:http://m.1010jiajiao.com/timu3_id_313847[举报]
Ⅰ.下列叙述正确的是.
A.“接触法”制H2SO4时,催化氧化阶段的反应原理为2SO2(g)+O2(g)
2SO3(g)△H<0
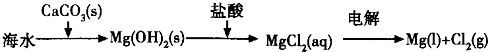
B.海水提镁的主要步骤为:
C.普通水泥的主要成分是硅酸钙
D.黏土的主要成分是三氧化二铝
Ⅱ.工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱.请回答下列问题:
(1)路布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取、结晶而制得纯碱.
①食盐和浓硫酸反应的化学方程式为
②硫酸钠和焦炭、石灰石反应的化学方程式为
(2)氨碱法的工艺如图1所示,得到的碳酸氢钠经煅烧生成纯碱.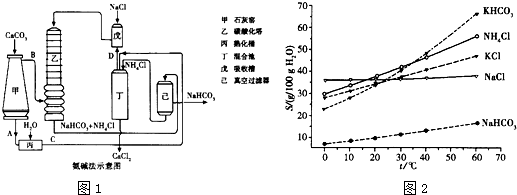
①图中的中间产物C是
②装置乙中发生反应的化学方程式为
(3)联合制碱法是对氨碱法的改进,其优点是
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石等为原料制碳酸钾.请结合图1的溶解度(S)随温度变化曲线,分析说明是否可行?
查看习题详情和答案>>
A.“接触法”制H2SO4时,催化氧化阶段的反应原理为2SO2(g)+O2(g)
| 催化剂 |
| △ |
B.海水提镁的主要步骤为:

C.普通水泥的主要成分是硅酸钙
D.黏土的主要成分是三氧化二铝
Ⅱ.工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱.请回答下列问题:
(1)路布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取、结晶而制得纯碱.
①食盐和浓硫酸反应的化学方程式为
2NaCl+H2SO4(浓)
Na2SO4+2HCl↑
| ||
2NaCl+H2SO4(浓)
Na2SO4+2HCl↑
;
| ||
②硫酸钠和焦炭、石灰石反应的化学方程式为
Na2SO4+2C+CaCO3
CaS+Na2CO3+CO2↑
| ||
Na2SO4+2C+CaCO3
CaS+Na2CO3+CO2↑
(已知产物之一为CaS);
| ||
(2)氨碱法的工艺如图1所示,得到的碳酸氢钠经煅烧生成纯碱.

①图中的中间产物C是
Ca(OH)2
Ca(OH)2
,D是NH3
NH3
(写化学式);②装置乙中发生反应的化学方程式为
CO2+H2O+NH3=NaHCO3↓+NH4Cl
CO2+H2O+NH3=NaHCO3↓+NH4Cl
;(3)联合制碱法是对氨碱法的改进,其优点是
能提高原料的利用率,减少废渣(CaCl2)的排放,保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高;
NH4Cl 可做氮肥;
可与合成氨厂联合,使合成氨的原料气 CO 转化成 CO2,革除了 CaCO3 制 CO2 这一工序
NH4Cl 可做氮肥;
可与合成氨厂联合,使合成氨的原料气 CO 转化成 CO2,革除了 CaCO3 制 CO2 这一工序
能提高原料的利用率,减少废渣(CaCl2)的排放,保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高;
NH4Cl 可做氮肥;
可与合成氨厂联合,使合成氨的原料气 CO 转化成 CO2,革除了 CaCO3 制 CO2 这一工序
;NH4Cl 可做氮肥;
可与合成氨厂联合,使合成氨的原料气 CO 转化成 CO2,革除了 CaCO3 制 CO2 这一工序
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石等为原料制碳酸钾.请结合图1的溶解度(S)随温度变化曲线,分析说明是否可行?
不可行.因为KHCO3和NH4Cl的溶解度相差不大,当温度高于40℃时,KHCO3的溶解度大于NH4Cl,降温结晶时会析出较多的KCl
不可行.因为KHCO3和NH4Cl的溶解度相差不大,当温度高于40℃时,KHCO3的溶解度大于NH4Cl,降温结晶时会析出较多的KCl
.(2013?烟台模拟)某课外活动小组根据Mg与CO2的反应原理,探究Mg与NO2的反应及固体产物.该小组通过实验确认Mg能在NO2中燃烧,并对固体产物提出三种假设:
I.固体产物为MgO;Ⅱ.固体产物为Mg3N2;III.固体.产物为
已知:2NO2+2NaOH=NaNO3+H2O;Mg3N2与水发生剧烈反应.
回答下列问题:
(1)利用下列仪器组装探究实验装置,按气流方向,正确的连接顺序是(每种仪器只用一次):
a接

(2)装置组装好后,检验气密性的方法是
(3)装置A中发生反应的离子方程式为
(4)装置C中盛装的干燥剂可以是(填序号)
①浓硫酸 ②无水CaCl2 ③碱石灰 ④五氧化二瞵
(5)实验开始时,先让A中反应进行一段时间,待B中充满红棕色气体后,再点燃B处酒精灯.这样做的目的是
(6)实验前镁粉的质量为12.00g,镁粉完全反应后得到的同一固体残留物称量了三次,所得数据分别是17.00g、18.02g、17.98go以上数据能否
(7)为了使测定结果更加准确,还需对组装好的装置进行的改进是
查看习题详情和答案>>
I.固体产物为MgO;Ⅱ.固体产物为Mg3N2;III.固体.产物为
固体为MgO和Mg3N2
固体为MgO和Mg3N2
.已知:2NO2+2NaOH=NaNO3+H2O;Mg3N2与水发生剧烈反应.
回答下列问题:
(1)利用下列仪器组装探究实验装置,按气流方向,正确的连接顺序是(每种仪器只用一次):
a接
d或e
d或e
,e或d
e或d
接b或c
b或c
,c或b
c或b
接g
g
.
(2)装置组装好后,检验气密性的方法是
对圆底烧瓶微热,若插入氢氧化钠溶液的导气管口处冒气泡,停止加热,该导气管中形成一段稳定水柱,表示气密性完好
对圆底烧瓶微热,若插入氢氧化钠溶液的导气管口处冒气泡,停止加热,该导气管中形成一段稳定水柱,表示气密性完好
.(3)装置A中发生反应的离子方程式为
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
.(4)装置C中盛装的干燥剂可以是(填序号)
②④
②④
.①浓硫酸 ②无水CaCl2 ③碱石灰 ④五氧化二瞵
(5)实验开始时,先让A中反应进行一段时间,待B中充满红棕色气体后,再点燃B处酒精灯.这样做的目的是
排净装置中的空气,防止空气干扰实验
排净装置中的空气,防止空气干扰实验
.(6)实验前镁粉的质量为12.00g,镁粉完全反应后得到的同一固体残留物称量了三次,所得数据分别是17.00g、18.02g、17.98go以上数据能否
不能
不能
(填“能”或“不能”)用托盘天平获得.通过计算判断以上假设Ⅲ
Ⅲ
是成立的.(7)为了使测定结果更加准确,还需对组装好的装置进行的改进是
在装置B和D之间连接一干燥装置
在装置B和D之间连接一干燥装置
.某一化学反应的实验装置如下图所示:
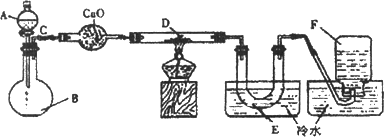
A~F属于F列物质中某一种:
浓硫酸、浓盐酸、浓氨水、锌粒、铜片、食盐、氧化钙、氧化铜、氮气、氧气、一氧化碳和水.
实验现象:
①D物质由黑色变为红色
②无水硫酸铜粉末放入无色透明的E中得到蓝色溶液
③燃着的镁带伸入无色无味的F中.镁带继续燃烧,生成一种灰黄色物质.将该物质放入水中,有气体放出,该气体能使润湿的红色石蕊试纸变蓝.通避分析回答:
(1)写出A~F中某些物质的名称:A________,F________;
(2)写出有关的化学方程式:C与D________;
F与Mg的反应产物与水的反应________.
(3)用上图中的气体发生器还可以制取氢气、二氧化碳、硫化氢等,问实验室条件下,能制取氧气和氯化氢吗?若能,请写出相应的反应方程式和文字表述;若不能,此空不填.
________;________.
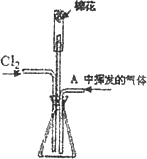
(4)见下图装置中试管口放置的棉花中应该浸有一种液体,这种液体是________,其作用是:________.