摘要:1]若X=0.Y=0.则Z= .[2]若X=0.75.Y= .Z= .
网址:http://m.1010jiajiao.com/timu3_id_313332[举报]
把0.6 mol X气体和0.4 mol Y气体混合于容积为2 L的容器中,使其发生如下反应:3 X(g)+Y(g)![]() nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
A.1 B.2
C.3 D.4
查看习题详情和答案>>把0.6 mol X气体和0.4 mol Y气体混合于容积为2 L的容器中,使其发生如下反应:3 X(g)+Y(g) nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
 nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )| A.1 | B.2 |
| C.3 | D.4 |
已知2X(g)+Y(g)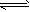 2Z(g) △H<0,在500℃时将2molX和1molY 装入一个体积恒定的10 L密闭容器中,
2Z(g) △H<0,在500℃时将2molX和1molY 装入一个体积恒定的10 L密闭容器中,
2 min (t1)时达到平衡,如下图所示。
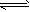 2Z(g) △H<0,在500℃时将2molX和1molY 装入一个体积恒定的10 L密闭容器中,
2Z(g) △H<0,在500℃时将2molX和1molY 装入一个体积恒定的10 L密闭容器中,2 min (t1)时达到平衡,如下图所示。
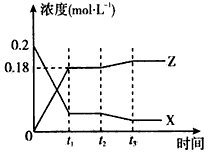
请回答下列问题:
(1)用Y表示2 min内该反应的平均反应速率为________,计算500℃时该反应的平衡常数K1=_________。
(2)某温度时该反应的平衡常数K2的数值为800,则此时的温度_______(填“大于”“小于”或“等于”)500℃。
(3)上图表示该反应在时刻t1时达到平衡后,时刻t2因改变某个条件而发生的变化情况,图中时刻t2发生改变的条件可能是____________ (只写一个条件)。
(4)500℃时,若起始装入的X、Y、Z分别为0.4 mol、amol、b mol,达到平衡时各组分的含量与题干中所达到的平衡完全相同,则a=_____mol,b=____mol,刚开始时反应向______反应方向进行(填“正”或“逆”)。
查看习题详情和答案>>
(1)用Y表示2 min内该反应的平均反应速率为________,计算500℃时该反应的平衡常数K1=_________。
(2)某温度时该反应的平衡常数K2的数值为800,则此时的温度_______(填“大于”“小于”或“等于”)500℃。
(3)上图表示该反应在时刻t1时达到平衡后,时刻t2因改变某个条件而发生的变化情况,图中时刻t2发生改变的条件可能是____________ (只写一个条件)。
(4)500℃时,若起始装入的X、Y、Z分别为0.4 mol、amol、b mol,达到平衡时各组分的含量与题干中所达到的平衡完全相同,则a=_____mol,b=____mol,刚开始时反应向______反应方向进行(填“正”或“逆”)。

