网址:http://m.1010jiajiao.com/timu3_id_310401[举报]
氯化铝为白色的粉末,遇潮湿空气极易吸收水分并部分水解放出氯化氢而形成酸雾,在183℃升华。工业上由金属铝和氯气作用或用碳氯化法可制得无水氯化铝。某课外兴趣小组在实验室中,通过下图装置制取少量纯净的无水氯化铝。
(1)装置A中用于盛装浓盐酸的仪器名称是 ,装置A可产生氯气和MnCl2溶液,该反应的化学方程式是 。
(2)装置B中盛放饱和NaCl溶液,该装置的主要作用是 。
(3)装置C、F均盛放浓硫酸,若取消装置C,则可能产生的不良影响是 。
(4)装置D中预期观察到的现象是剧烈燃烧,发出白光, 。
(5)另选一件仪器装入适当试剂后,也可起到F和G的作用,所装填的试剂名称为 。
(6)工业碳氯化法制无水氯化铝是对氧化铝、碳和氯气进行加热,可得副产品一氧化碳,该反应的化学方程式是 。
氯化铝为白色的粉末,遇潮湿空气极易吸收水分并部分水解放出氯化氢而形成酸雾,在183℃升华。工业上由金属铝和氯气作用或用碳氯化法可制得无水氯化铝。某课外兴趣小组在实验室中,通过下图装置制取少量纯净的无水氯化铝。

(1)装置A中用于盛装浓盐酸的仪器名称是 ,装置A可产生氯气和MnCl2溶液,该反应的化学方程式是 。
(2)装置B中盛放饱和NaCl溶液,该装置的主要作用是 。
(3)装置C、F均盛放浓硫酸,若取消装置C,则可能产生的不良影响是 。
(4)装置D中预期观察到的现象是剧烈燃烧,发出白光, 。
(5)另选一件仪器装入适当试剂后,也可起到F和G的作用,所装填的试剂名称为 。
(6)工业碳氯化法制无水氯化铝是对氧化铝、碳和氯气进行加热,可得副产品一氧化碳,该反应的化学方程式是 。
查看习题详情和答案>>

(1)装置A中用于盛装浓盐酸的仪器名称是 ,装置A可产生氯气和MnCl2溶液,该反应的化学方程式是 。
(2)装置B中盛放饱和NaCl溶液,该装置的主要作用是 。
(3)装置C、F均盛放浓硫酸,若取消装置C,则可能产生的不良影响是 。
(4)装置D中预期观察到的现象是剧烈燃烧,发出白光, 。
(5)另选一件仪器装入适当试剂后,也可起到F和G的作用,所装填的试剂名称为 。
(6)工业碳氯化法制无水氯化铝是对氧化铝、碳和氯气进行加热,可得副产品一氧化碳,该反应的化学方程式是 。
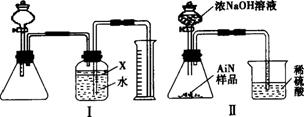
(1)实验有关操作为:a.往锥形瓶中放入适量的AlN样品;b.从分液漏斗往锥形瓶中加入过量的浓NaOH;c.检查装置的气密性;d.测定收集到水的体积。正确的操作顺序为_____________。
(2)本试验中检查装置气密性的方法是______________。
(3)广口瓶中的试剂X可选用___________(填选项序号)。
A.汽油 B.酒精 C.植物油 D.四氯化碳
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将____________(填“偏大”“偏小”或“不变”)。
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是__________________。
(6)若实验中测得样品的质量为w g,氨气的体积为a L(标准状况),则样品中AlN的质量分数为_______________(AlN的相对分子质量为41)。
(7)有人改用图Ⅱ装置进行同样的实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数。你认为是否可行____________(填“可行”或“不可行”),原因是_________________,改进的方法是___________________________________________________________________。
查看习题详情和答案>>(20分)聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭 土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
已知:Fe3+、Al3+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2。
根据流程图回答下列问题:
(1)“煅烧”的目的是_______________________________________________。
(2)“浸出”过程中发生反应的离子方程式为_______________________________。
(3)“浸出”选用的酸为_______。配制质量分数15%的A酸需要200mL30%的A酸(密度约为1.15g/cm3)和_______g蒸馏水,配制用到的仪器有烧杯、玻璃棒、______________。
(4)为提高铝的浸出率,可采取的措施有 _______________(要求写出三条)。
(5)“调节溶液pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是_________________;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是___________ ______。
(6)实验中制备碱式氯化铝反应的化学方程式为_________________
查看习题详情和答案>>