摘要:28.推断: 熔融 浓H2SO4 电解 氧化物A 单质B 难溶 △ 气体E 浓盐酸 NaOH溶液 NaHCO3溶液 D △ MnO2 单质C 沉淀F 溶解 HCl溶液 (1)A是 .B是 .D是 .E是 , (2)写出下列反应的化学方程式: MnO2 + 浓盐酸: 沉淀F + NaOH溶液:
网址:http://m.1010jiajiao.com/timu3_id_308881[举报]
现代工业上用氨与二氧化碳在高压下反应,先生成氨基甲酸铵,再脱水生成尿素.反应式为
2NH3+CO2
NH2COONH4;NH2COONH4?CO(NH2)2+H2O根据已学知识推断起固氮作用的化学反应是
( )
2NH3+CO2
| 高压 |
( )
| A、NO2与H2O的反应生成HNO3和NO | |||
| B、NO与O2反应生成NO2 | |||
| C、NH3经催化氧化生成NO | |||
D、N2
|
 X、Y、Z三种可溶性盐,其阳离子分别Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl-、SO42-、NO3-中的某一种.现做以下实验:
X、Y、Z三种可溶性盐,其阳离子分别Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl-、SO42-、NO3-中的某一种.现做以下实验:①将三种盐各取少量,分别溶于盛有5mL蒸馏水的三支试管中,只有X盐溶液呈蓝色.
②分别向三支试管中加入2mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象.
(1)根据上述事实,推断这四种盐的化学式分别为:
X
CuSO4
CuSO4
YAgNO3
AgNO3
ZBaCl2
BaCl2
(2)若上述三种阳离子Ba2+、Cu2+、Ag+对应的盐都为硝酸盐,将其混合配成溶液,选择合适试剂,将这三种离子逐一沉淀分离.其流程图如图:
部分物质溶解性表
| Ba2+ | Cu2+ | Ag+ | |
| Cl- | 溶 | 溶 | 不 |
| CO 32- | 不 | 不 | 不 |
| SO 42- | 不 | 溶 | 不 |
| S2- | 溶 | 不 | 不 |
AgCl
AgCl
.②写出混合液+A的离子方程式
Ag++Cl-═AgCl↓
Ag++Cl-═AgCl↓
.③若C为Na2S,且它与B属于同一类盐,则B试剂的名称是
硫酸钠
硫酸钠
.硫酸氢钠
硫酸氢钠
.下列有关物质分类的叙述正确的是( )
| A、根据金属铜能导电可判断:铜为电解质 | B、根据分类的观点可判断:纯碱属于碱类 | C、根据分散质粒子的直径大小可区分:胶体和溶液 | D、根据都能使有色物质褪色这一现象推断:氯水和活性炭的漂白原理相同 |
今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按下图方式进行转化:

其推断正确的是( )

其推断正确的是( )
| 选项 | 甲 | 乙 | 丙 | 丁 | 戊 |
| A | NH3 | O2 | NO | H2O | NO2 |
| B | Mg | CO2 | C | MgO | CO |
| C | C | H2O | CO | H2 | HCOOH |
| D | FeBr2 | Cl2 | FeCl2 | Br2 | FeCl3 |
| A、A | B、B | C、C | D、D |
 (2009?佛山一模)10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如下变化:
(2009?佛山一模)10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如下变化:| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
;(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
大于
大于
(填“大于”或“小于”)NaHCO3;(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH
=
=
8.3(填“>”、“<”或“=”),说明甲正确,若pH>
>
8.3(填“>”、“<”或“=”),说明乙正确;(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:
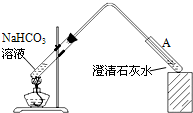
实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明
乙
乙
(填“甲”或“乙”)推测正确;(5)将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此资料可以判断
乙
乙
(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成
溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成
.