摘要:28.A.B.C.D四种短周期元素原子序数依次增大.A元素原子的价电子排列为ns2np2.B元素的最外层电子数是其电子层数的3倍.E元素原子的价电子排布为3d64s2.C.D的电离能数据如下(kJ·mol―1): I1 I2 I3 I4 C 738 1451 7733 10540 D 577 1817 2745 11578 (1)化合价是元素的一种性质.由C.D的电离能数据判断.C通常显 价.D显 价, (2)某单质甲分子与化合物AB分子中电子总数相等.则甲分子中包含 个σ键. 个π键, (3)AB的总键能大于甲的总键能.但AB比甲容易参加化学反应.根据下表数据.说明AB比甲活泼的原因是 单键 双键 叁键 AB 键能(kJ·mol―1) 357.7 798.9 1071.9 甲 键能(kJ·mol―1) 154.8 418.4 941.7 (4)E能与AB形成配合物.其中E提供 .AB提供 . (5)下列晶胞中.阳离子与阴离子的个数为
网址:http://m.1010jiajiao.com/timu3_id_305970[举报]
A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2.C、D的电离能数据如下(kJ?mol-1):
(1)化合价是元素的一种性质.由C、D的电离能数据判断,C通常显
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是
 (4)E能与AB形成配合物,其中E提供
(4)E能与AB形成配合物,其中E提供
(5)如图所示晶胞中,阳离子与阴离子的个数为
查看习题详情和答案>>
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
+2
+2
价,D显+3
+3
价;(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含
1
1
个σ键,2
2
个π键;(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是
断裂C≡O中的一个π键消耗的能量是273kJ/mol,断裂N≡N中的一个π键消耗的能量是523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼
断裂C≡O中的一个π键消耗的能量是273kJ/mol,断裂N≡N中的一个π键消耗的能量是523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼
.| 单键 | 双键 | 叁键 | ||
| AB | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ?mol-1) | 154.8 | 418.4 | 941.7 |
 (4)E能与AB形成配合物,其中E提供
(4)E能与AB形成配合物,其中E提供空轨道
空轨道
,AB提供孤对电子
孤对电子
.(5)如图所示晶胞中,阳离子与阴离子的个数为
3:1
3:1
.A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2.C、D的电离能数据如下(kJ?mol-1):
(1)化合价是元素的一种性质.由C、D的电离能数据判断,C通常显______价,D显______价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含______个σ键,______个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是______.
 (4)E能与AB形成配合物,其中E提供______,AB提供______.
(4)E能与AB形成配合物,其中E提供______,AB提供______.
(5)如图所示晶胞中,阳离子与阴离子的个数为______.
查看习题详情和答案>>
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含______个σ键,______个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是______.
| 单键 | 双键 | 叁键 | ||
| AB | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ?mol-1) | 154.8 | 418.4 | 941.7 |
 (4)E能与AB形成配合物,其中E提供______,AB提供______.
(4)E能与AB形成配合物,其中E提供______,AB提供______.(5)如图所示晶胞中,阳离子与阴离子的个数为______.
A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ·mol―1):
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显 价,D显 价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含___个σ键,___个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是______________________________
| 单键 | 双键 | 叁键 | ||
| AB | 键能(kJ·mol―1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ·mol―1) | 154.8 | 418.4 | 941.7 |
(4)E能与AB形成配合物,其中E提供______________,AB提供________________。
(5)下列晶胞中,阳离子与阴离子的个数为
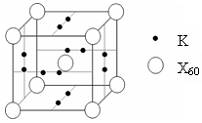
(9分)A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ·mol―1):
| | I1 | I2 | I3 | I4 |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显 价,D显 价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含___个σ键,___个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是______________________________
| | 单键 | 双键 | 叁键 | |
| AB | 键能(kJ·mol―1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ·mol―1) | 154.8 | 418.4 | 941.7 |
(4)E能与AB形成配合物,其中E提供______________,AB提供________________。
(5)下列晶胞中,阳离子与阴离子的个数为
 查看习题详情和答案>>
查看习题详情和答案>>
(9分)A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ·mol―1):
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显 价,D显 价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含___个σ键,___个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是______________________________
(4)E能与AB形成配合物,其中E提供______________,AB提供________________。
(5)下列晶胞中,阳离子与阴离子的个数为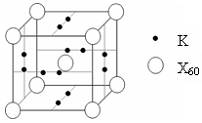
| | I1 | I2 | I3 | I4 |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显 价,D显 价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含___个σ键,___个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是______________________________
| | 单键 | 双键 | 叁键 | |
| AB | 键能(kJ·mol―1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ·mol―1) | 154.8 | 418.4 | 941.7 |
(4)E能与AB形成配合物,其中E提供______________,AB提供________________。
(5)下列晶胞中,阳离子与阴离子的个数为
