摘要:26.在实验室里制取乙烯.常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫.有人设计下列实验图以确认上述混合气体中有C2H4和SO2. (1)I.II.III.IV装置可盛放的试剂是I ,II ,III ,IV (将下列有关试剂的序号填入空格内), A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.酸性KMnO4溶液 (2)能说明SO2气体存在的现象是 , (3)使用装置II的目的是 , (4)使用装置III的目的是 , (5)确定含有乙烯的现象是 .27.某化学实验小组采用类似制乙酸乙酯的装置.以环己醇制备环己烯. 已知: 密度(g/cm3) 熔点(℃) 沸点(℃) 溶解性 环己醇 0.96 25 161 能溶于水 环己烯 0.81 -103 83 难溶于水 (1)制备粗品 将12.5mL环己醇加入试管A中.再加入1mL浓硫酸.摇匀后放入碎瓷片.缓慢加热至反应完全.在试管C内得到环己烯粗品. ①A中碎瓷片的作用是 .导管B除了导气外还具有的作用是 , ②试管C置于冰水浴中的目的是 . (2)制备精品 ①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水.振荡.静置.分层.环己烯在 层.分液后用 洗涤. A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液 ②再将环己烯按上右图装置蒸馏.冷却水从 口进入.蒸馏时要加入生石灰.目的是 . ③收集产品时.温度应控制在 左右.实验制得的环己烯精品质量低于理论产量.可能的原因是 , A.蒸馏时从70℃开始收集产品 B.环己醇实际用量多了 C.制备粗产品时环己醇随产品一起蒸出 (3)以下区分环己烯精品和粗品的方法.合理的是 ( ) A.用酸性高锰酸钾溶液 B.用金属钠 C.测定沸点
网址:http://m.1010jiajiao.com/timu3_id_305393[举报]
 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验如图以确认上述混合气体中有C2H4和SO2.回答下列问题:
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验如图以确认上述混合气体中有C2H4和SO2.回答下列问题:(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:Ⅰ
A
A
;ⅡB
B
;ⅢA
A
;ⅣD
D
(将下列有关试剂的序号填入空格内).A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
装置Ⅰ中品红褪色
装置Ⅰ中品红褪色
.(3)使用装置Ⅱ的目的是
除去二氧化硫以免干扰乙烯的检验
除去二氧化硫以免干扰乙烯的检验
.(4)使用装置Ⅲ的目的是
检验二氧化硫是否被完全除去
检验二氧化硫是否被完全除去
.(5)确定含有乙烯的现象是
装置Ⅲ中品红不褪色,装置Ⅳ中高锰酸钾溶液褪色
装置Ⅲ中品红不褪色,装置Ⅳ中高锰酸钾溶液褪色
.在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,为了检验SO2和C2H4的性质,有人设计下列实验方案.

(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是I
A.品红溶液 B.NaOH溶液
C.浓H2SO4 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
(3)使用装置Ⅱ的目的是
(4)确定含有乙烯的现象是
(5)如果Ⅳ盛放的溶液为溴水,那么发生的化学方程式为
查看习题详情和答案>>

(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是I
A
A
;ⅡB
B
;ⅢA
A
;ⅣD
D
(将下列有关试剂的序号填入空格内);A.品红溶液 B.NaOH溶液
C.浓H2SO4 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
装置Ⅰ中品红溶液褪色
装置Ⅰ中品红溶液褪色
;(3)使用装置Ⅱ的目的是
除去二氧化硫气体,以免干扰乙烯的实验
除去二氧化硫气体,以免干扰乙烯的实验
;(4)确定含有乙烯的现象是
装置Ⅲ中的品红溶液不褪色,装置Ⅳ中的酸性高锰酸钾溶液褪色
装置Ⅲ中的品红溶液不褪色,装置Ⅳ中的酸性高锰酸钾溶液褪色
.(5)如果Ⅳ盛放的溶液为溴水,那么发生的化学方程式为
CH2=CH2+Br2→CH2Br-CH2Br
CH2=CH2+Br2→CH2Br-CH2Br
,反应类型为加成
加成
. 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计如图实验以确认上述混合气体中有C2H4和SO2.
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计如图实验以确认上述混合气体中有C2H4和SO2.(1)写出实验室制备乙烯的化学方程式:
CH3CH2OH
CH2=CH2↑+H2O
| 浓硫酸 |
| 170℃ |
CH3CH2OH
CH2=CH2↑+H2O
其中浓硫酸的作用是| 浓硫酸 |
| 170℃ |
催化剂、脱水剂
催化剂、脱水剂
圆底烧瓶中加入碎瓷片的作用是防止防止暴沸
防止暴沸
(2)I、II、III、IV装置可盛放的试剂是I
A
A
;IIB
B
;IIIA
A
;IVD
D
(将下列有关试剂的序号填入空格内);A.品红溶液 B.NaOH溶液 C.浓H2SO4D.酸性KMnO4溶液
(3)能说明SO2气体存在的现象是
Ⅰ中品红褪色
Ⅰ中品红褪色
;(4)使用装置II的目的是
吸收SO2
吸收SO2
;(5)使用装置III的目的是
检验SO2是否已经被完全吸收
检验SO2是否已经被完全吸收
;(6)确定含有乙烯的现象是
Ⅲ中的品红不褪色,Ⅳ中的高锰酸钾溶液褪色
Ⅲ中的品红不褪色,Ⅳ中的高锰酸钾溶液褪色
.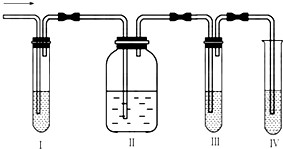 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2.
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2. 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计实验图以确认上述混合气体中有C2H4和SO2.回答下列问题:
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计实验图以确认上述混合气体中有C2H4和SO2.回答下列问题: