网址:http://m.1010jiajiao.com/timu3_id_305340[举报]
(10分,每空2分)
漂白粉可以和浓盐酸反应产生氯气,某课外兴趣小组试图测定氯气的体积并验证纯净干燥的氯气没有漂白性,现用如图所示装置进行实验,请回答有关问题: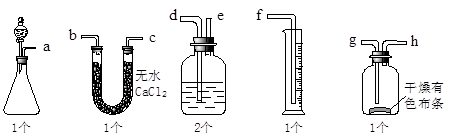
(1)该装置的正确连接顺序是:a接( )、( )接( )、( )接( )、( )接( )、( )接( )。
(2)U型管可以用内盛装__________的洗气瓶代替
(3)在制取氯气前,必须进行的一项操作步骤是__________________
(4)按照实验目的进行之后,干燥有色布条是否褪色( )(填是或否)。
(5)该兴趣小组在实验中,发现量筒中并没有收集到液体,你认为他们失败的原因可能是____________________________________________________。
(10分,每空2分)
漂白粉可以和浓盐酸反应产生氯气,某课外兴趣小组试图测定氯气的体积并验证纯净干燥的氯气没有漂白性,现用如图所示装置进行实验,请回答有关问题:

(1)该装置的正确连接顺序是:a接( )、( )接( )、( )接( )、( )接( )、( )接( )。
(2)U型管可以用内盛装__________的洗气瓶代替
(3)在制取氯气前,必须进行的一项操作步骤是__________________
(4)按照实验目的进行之后,干燥有色布条是否褪色( )(填是或否)。
(5)该兴趣小组在实验中,发现量筒中并没有收集到液体,你认为他们失败的原因可能是____________________________________________________。
查看习题详情和答案>>
漂白粉可以和浓盐酸反应产生氯气,某课外兴趣小组试图测定氯气的体积并验证纯净干燥的氯气没有漂白性,现用如图所示装置进行实验,请回答有关问题:
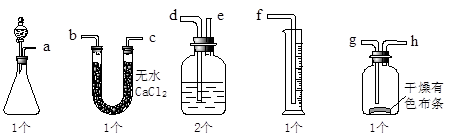
(1)该装置的正确连接顺序是:a接( )、( )接( )、( )接( )、( )接( )、( )接( )。
(2)U型管可以用内盛装__________的洗气瓶代替
(3)在制取氯气前,必须进行的一项操作步骤是__________________
(4)按照实验目的进行之后,干燥有色布条是否褪色( )(填是或否)。
(5)该兴趣小组在实验中,发现量筒中并没有收集到液体,你认为他们失败的原因可能是____________________________________________________。
①把甲酸(HCOOH)和足量的NaOH溶液混合;
②用Na2SO3固体和某酸反应制备SO2气体;
③在一定温度下,将足量的SO2气体通入①的溶液中,即有保险粉生成,同时生成一种气体。
(1)写出NaOH的电子式
(2)制备SO2时所选用的酸,你认为下列最适宜选用的是
| A.浓盐酸 | B.质量分数为70%的H2SO4 |
| C.稀硝酸 | D.质量分数为10%的稀硫酸 |
(4)保险粉可以用于除去废水中的重铬酸根离子(Cr2O72-被转化为Cr3+),这是目前除去酸性废水中铬离子的有效方法之一,则每消耗0.1mol保险粉,理论上可以除去Cr2O72-的物质的量为 mol。
(5)保险粉不稳定,容易分解生成甲、 乙、 丙三种化合物。若将甲、乙两种物质分别配成溶液,在甲溶液中加入稀硫酸,则有淡黄色沉淀和气体丙产生;乙溶液中加入BaCl2溶液和稀盐酸,有气体丙产生,但无白色沉淀。
在甲溶液中加入稀硫酸后所发生反应的离子方程式为
保险粉分解的化学方程式为
(6)保险粉在空气中容易吸收氧气而发生氧化。其方程式为:
①2Na2S2O4+O2+H2O==4NaHSO3或②2Na2S2O4+O2+H2O==4NaHSO3+NaHSO4
请设计实验证明氧化时发生的是②的反应。
 (08上海模拟)某活动课程小组拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
(08上海模拟)某活动课程小组拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
a.取25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸溶液1~2 min;
c.在得到的溶液中加入另一半(25mL)NaOH溶液,使其充分混合反应。
(1)此方案能制得较纯净的Na2CO3,写出a、c两步的化学反应方程式 ____________________、____________________________。
此方案第一步的实验装置如下图所示:
(2)加入反应物前,如何检查整个装置的气密性________________________________________。
(3)装置B中盛放的试剂是______________,作用是_______________________________。
 (4)在实验室通常制法中,装置A还可作为下列_____________气体的发生装置(填序号)。
(4)在实验室通常制法中,装置A还可作为下列_____________气体的发生装置(填序号)。
①CH2==CH2 ②H2S ③CH4 ④CH≡CH ⑤H2
(5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4, ⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
(6)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶 液密度为1.44 g / mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为____________________。
查看习题详情和答案>>